*Guillermo J Aramburú, *Alejandra C Aguzzi, *Verónica E Ricco, *Sergio A Hubert, **Javier Aguilar, **Brenda Konigheim, *Carolina M Virga.
*Cátedra de Farmacología y Terapéutica B Facultad de Odontología - UNC
**Instituto de Virología - UNC -Brasil
Correspondencia:
Dra. María Carolina Virga. Haya de la Torre s/n, estafeta 32, CP 5016. Facultad de Odontología. Ciudad Universitaria. Córdoba
E-mail: [email protected]
Resumen: |
Introducción:
Diversas situaciones fisiológicas o patológicas inducen la pérdida de tejido óseo. En tal sentido, se han propuesto diferentes biomateriales y drogas que serían capaces de desencadenar procesos biológicos, para iniciar la recuperación de tejido óseo perdido.
Los bisfosfonatos, también denominados difosfonatos o bifosfonatos, son fármacos, de gran utilidad en el diagnóstico y tratamiento de ciertas enfermedades metabólicas óseas. Estos fármacos constituyen una de las innovaciones terapéuticas más importantes de los últimos años en el control de la osteoporosis y de la enfermedad ósea de Paget. (1-3 )
Actúan como inhibidores específicos de la reabsorción ósea mediada por osteoclastos. Son análogos estructurales a los pirofosfatos del hueso, reemplazando el oxígeno de su estructura química por carbono. Esta estructura es completamente resistente a la destrucción enzimática a nivel de la unión P-C-P. Al igual que el pirofosfato, tienen una alta afinidad por el hueso mineral, y una vez absorbidos estas drogas son incorporadas a la matriz ósea. (4-6)
Se sabe que el tratamiento con estas drogas aumenta la producción de hueso es decir, el números de sitios en los que el hueso se remodela además, la formación del hueso supera la resorción en estos sitios remodelados, y como consecuencia de ello se producen ganancias progresivas en la masa ósea. (7-8)
La habilidad de los bifosfonatos para unirse a los cristales y prevenir su disolución fue reforzado cuando el sitio R1 de su estructura química fue modificado introduciéndole un grupo hidroxilo (en el caso de Etidronato), o un átomo de halógeno tales como el cloro (en el caso del Clodronato).
Esto se debe, al menos en parte, al hecho de que la presencia del grupo hidroxilo en la posición R1 aumenta la afinidad por el calcio en consecuencia la mineralización ósea favoreciendo la capacidad de estas drogas por quelar iones. La marcada selectividad de los bifosfonatos por el hueso más que por otros tejidos le da valor en la práctica clínica. Los de última generación representan los más potentes bifosfonatos ya que en su estructura química contienen nitrógeno, como el Alendronato y Risendronato Los integrantes de este grupo interfieren con reacciones metabólicas en el curso de la biosíntesis del mevalonato (precursor del colesterol) pudiendo afectar la actividad celular intefiriendo con proteínas. (9-10) Por estas razones se escoge Alendronato como droga para la investigación.
Al unirse a las sales de calcio, el Alendronato bloquea la transformación de fosfato de calcio a hidroxiapatita por lo tanto inhibe la formación, agregación y disolución de los cristales del hueso. (11-12)
A nivel celular, el Alendronato actúa de manera preferencial en los sitios de reabsorción ósea, a nivel del citoesqueleto de los osteoclastos, provocando pérdida del borde en cepillo, aunque no interfiere en el reclutamiento y adhesión osteoclástica.
Se ha propuesto que esta droga mejoraría la calidad ósea mediante la asociación a los cristales de hidroxiapatita. Concomitantemente, es capaz de inhibir la actividad osteoclástica, disminuyendo por lo tanto la resorción ósea.
Esta situación modificaría el balance que se conoce opera en el mecanismo de resorción y formación ósea. Sin embargo no se ha descripto el efecto que el Alendronato ejercería sobre el hueso en el proceso de regeneración ósea. (13-17)
Esta investigación tiene como objetivo desarrollar una nueva formulación en base a alendronato para ser aplicada en forma subcutánea, ya que no existe en el mercado, e investigar sus efectos sobre un defecto óseo creado experimentalmente.
Materiales y métodos:
Preparación de la formulación
La fórmula farmacéutica se preparó con una dosificación de 0,5 mg de alendronato por Kg de peso, en una concentración de 0,875mg/5 ml; se le adisionó Cloruro de Na 43,84 mg., Citrato de Na 3,61 mg. Y agua para inyectable c.s.p. 5 ml, el pH final fue de 5,5 en medios estériles. El control fueron buffers sin principios activos.
Curvas de citotoxicidad
Tanto a la droga en estado puro como a la formulación se les realizó curvas de citotoxicidad, para comprobar la efectividad tanto de la droga en estado puro como a la formulación descartando efectos adversos. Este estudio se realiza por medio del Neutral Red Uptake Method (NR Sigma), basado en la capacidad de las células viables de incorporar y de fijar el rojo neutral, un tinte supravital. NR. Es un tinte catiónico débil que penetra fácilmente las membranas de las células por difusión no iónica, acumulándose a nivel intracelular en los lisosomas, donde se fija con los sitios aniónicos en la matriz lisosomal. Las alteraciones de la superficie de la célula o de la membrana lisosomal sensible conducen a la fragilidad lisosomal y a otros cambios que llegan a ser gradualmente irreversibles. Es posible así distinguir entre células viables, dañadas o muertas. De esta manera, la viabilidad celular se basó en la medida de la inhibición del crecimiento celular provocada por la sustancia objeto de estudio, empleando rojo neutro, colorante vital que es absorbido por las células vivas. Las muestras se observaron a través de microscopiode fase de contraste. También el material fue analizado por densidad óptica, a una longitud de onda 546:1 nm, siendo el de referencia 404 nm. El material fue incubado a 37°C. (18)
Experimentación con animales
Se tomaron 18 ratas Wistar machos adultas jóvenes (n=18), con un peso promedio de 150 gr., las cuales serán intervenidas quirúrgicamente en sus patas traseras. Previa anestesia general con una solución de Ketamina (8 mg.) y Xilazina (1,28 mg.) por 100 gr. de peso corporal, se depilaron y desinfectaron la región tibial con una solución de Cloruro de Benzalconio. Se realizó una insición con bisturí Nº 15, y posteriormente, se decoló disecando la facia subcutánea, los músculos y ligamentos, con el fin de exponer la superficie externa de las tibias, en el área de la diáfisis ósea, según el modelo descripto por Cabrini y col.(Laminar test) (19) Se realizó una cavidad de 1,5 mm de diámetro hasta llegar al hueso medular, con una fresa de carburo tungsteno, redonda de extremo cortante (Nº6), mediante rotación manual para prevenir el sobrecalentamiento del hueso, con el probable daño tisular.
Los animales fueron divididos en dos grupos según el siguiente diseño experimental:
Grupo 1: (grupo experimental) la cavidad ósea fue realizada y se inyectó Alendronato por vía subcutánea, a los Tiempos (T) 0, 7, 15 y 30 días. (T0: inmediatamente luego de la intervención quirúrgica) (n:16)
Grupo 1-a: Inyectado a T0, sacrificado T 0. (n:4)
Grupo 1-b: Inyectado a T0, sacrificado a 7 días. (n:4)
Grupo 1-c: Inyectado a T0 y T7 y sacrificado a los 15 días. (n:4)
Grupo 1-d: Inyectado a T0, T7, T14 sacrificado a los 30 días. (n:4)
Grupo 2: (grupo control) las cavidades logradas sólo fueron cubierta con el coágulo generado por la intervención quirúrgica. Se inyectó solución sin principios activos inmediatamente posterior a la cirugía, a los T 0, 7, 15 y 30 días. Se hicieron subgrupos equivalentes a los del grupo 1.
En ambos Grupos, luego de realizadas las intervenciones quirúrgicas, se recolocaron los planos en posición, y se suturaron las heridas con hilo reabsorbible. Los animales fueron tratados según normas universales de asepsia y no se administró otro tratamiento farmacológico.
Los animales fueron mantenidos en jaulas con dieta balanceada y agua ad libitum, durante el período de tiempo experimental. Los animales sacrificados por inhalación de éter en los tiempos experimentales. El tratamiento de los animales fue realizado respetando las normas de la Declaración de Helsinki de 1975 para el trabajo sobre animales de laboratorio.
Estudios radiográficos
Se tomaron radiografías pre y post quirúrgicas, evaluando las mismas cuantitativamente mediante la técnica de la densitometría ósea (DMO), y cualitativamente mediante la escala de graduación de imágenes radiográficas diseñada por Bornancini, C.A. (20) También fueron analizadas mediante un analizador de imagen según el programa " Image Pto Plus".
Estudios estadísticos:
Los medios del grupo fueron comparados por el análisis de la variación (ANOVA) seguido por una comparación múltiple de medios de Student-Newman-Keuls-Newman-Keuls. Sobre suceso la comparación de medios por la prueba de T-Student fue utilizada. p < 0,05 era considerado significativo.
Resultados:
Curvas de citotoxicidad
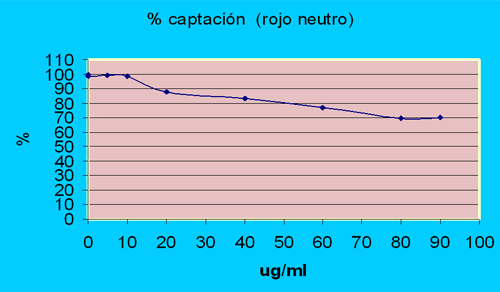
El Figura 1 muestra que el alendronato a bajas concentraciones (menos de 10 g/ml) presenta una viabilidad celular superior al 98%; al aumentar las concentraciones de droga, las células comienzan a verse afectadas, pero la viabilidad nunca baja del 70%. Esto puede deberse a que a mayores concentraciones el alendronato precipite, o puede ser que antes de que el alendronato precipite, se sature la entrada del mismo a la célula. De los resultados obtenidos se puede apreciar que el rango de trabajo con el alendronato puede tomarse desde 0 a 20 g/ml con toxicidad casi nula para las células, entre 20 y 60 g/ml entramos en una zona subtóxica, y más de 60 g/ml en una zona de baja toxicidad.
Estudios radiográficos
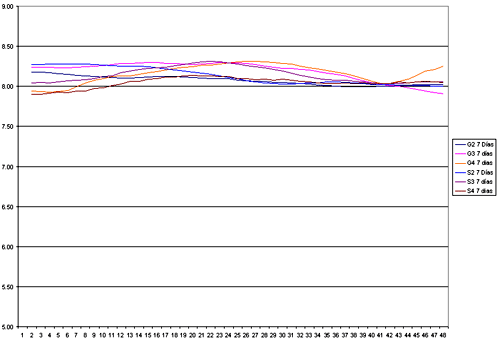
La Figura 2, muestra el nivel de radiopacidad de radiografías tomadas a las muestras en los (T) experimentales. Cabe destacar que el número mas alto indica mayor radioluminosidad. Se observa claramente el incremento de material radiopaco a medida que pasa el tiempo, llegando a los 30 días a no distinguirse claramente, el lugar de la incisión. Esta situación se observa en todos los casos estudiados Las Rx muestran diferencias estadísticamente significativas (p=0,05) entre los dos grupos, observándose formación ósea en cuanto a volumen.
| Radiografías: | |||||
| A | 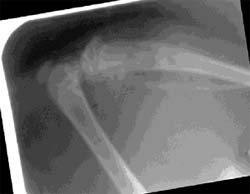 |
B | 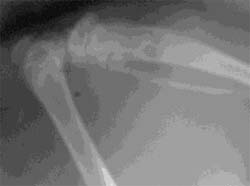 |
||
| Control día 0. | Control día 7. | ||||
| C | 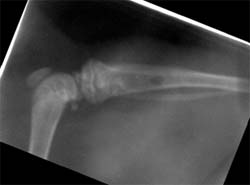 |
D |  |
||
| Problema día 7. | Image Plus día 7. | ||||
| E | 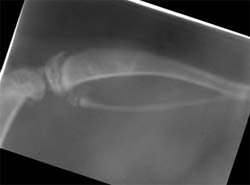 |
F |  |
||
| Problema día 30. | Image Plus día 30. | ||||
Discusión:
El alendronato es un potente inhibidor de la resorción ósea, sin presentar interferencia en la formación del hueso. Este tipo de drogas se utilizan como coadyuvantes en el tratamiento de diversas patologías en las que se ve involucrada la destrucción del hueso tales como enfermedad de Pagets (21-22), hipercalcemia tumoral, metástasis ósea (23-24) y osteoporosis inmovilizante. (25) El tratamiento diario con alendronato oral durante 3 años dio como resultado un aumento de la densidad ósea de huesos como columna vertebral, cadera y el total del hueso corporal en mujeres con osteoporosis postmenopausia, y estos efectos asociados con reducción de fracturas vertebrales, anomalías de forma, pérdida de altura y en gran parte la disminución en las fracturas en otros sitios del cuerpo. (4)
En la clínica dental hay pacientes que reciben una variedad terapéutica que influye directamente en su esqueleto. Entre estas medicaciones podemos citar quimioterapéuticos, agentes inmunosupresores, esteroides, antiinflamatorios no esteroideos. Esta terapéutica puede ejercer influencias en los niveles celulares y moleculares con alteraciones significativas en la fisiología del hueso del ambiente bucal.
La biocompatibilidad se puede definir como la capacidad de un material de funcionar en un uso específico en la presencia de una respuesta apropiada del huésped. (26) La necesidad de drogas biocompatibles, sin efectos secundarios, implica la necesidad de la prueba de la toxicidad. La toxicidad de una droga se puede evaluar por las pruebas in- vitro, y por estudios clínicos en seres humanos. Los estudios in-vitro son realizadas principalmente para evaluar la citotoxicidad (daños de la célula) o la genotoxicidad (el daños específica de la DNA o aberración cromosómica) de una droga. La prueba de NR se considera un método rápido, válido y reproductivo para evaluar la citotoxicidad in vitro. En este estudio, según lo determinado por la formulación con alendronato, la prueba de NR demostró no ser citotóxico después del uso en línea de la célula del fibroblasto.
Tanto la droga en estado puro (principio activo) como la formulación (Innovación farmacológica), preparada a bajas concentraciones su viabilidad es mayor al 98%, al aumentar la concentración de la droga las células comienzan a verse afectadas. Se observan alteraciones en la superficie de la célula y la membrana lisosomal sensible que conducen a la fragilidad lisosomal y a otros cambios que llegan a ser gradualmente irreversibles; pero la viabilidad nunca baja del 70%, por más que se siga agregando droga. De los resultados obtenidos se desprende que el alendronato puede usarse para los distintos ensayos en concentraciones que van de 0 a 90 g/ml sin que se produzcan alteraciones o daños visibles en las células.
Estudios experimentales previos (27) han demostrado que la aplicación tópica de una dosis de 200 ?g de alendronato colocado en el sitio de la cirugía mucoperióstica reduce la cantidad total de la resorción del hueso alveolar. Diversos autores han demostraron también el efecto de diferentes bisfosfonatos, administrados sistémica o localmente, en la recuperación de los niveles óseos posterior a la cirugía mucoperióstica utilizando el mismo método de evaluación. (28-29) En concordancia, el presente estudio ha demostrado un significado incremento del material radiopaco del hueso en los animales que recibieron alendronato, en comparación con el grupo que sólo recibió buffer, llegando a los 30 días a no distinguirse claramente el lugar de la incisión. La efectividad del tratamiento de alendronato, en dosis de 0,5 mg/Kg de peso corporal, es medible en los diversos cambios producidos a nivel de la pérdida ósea produciéndose un incremento en el porcentaje de hueso con características de normalidad. Cuando el alendronato fue aplicado cercano al sitio de la cirugía, la dosis utilizada como lo indica el fabricante fue significantemente efectiva (p<0,001) en incrementar los niveles óseos. También pudimos observar que la administración subcutánea es significativamente efectiva en los tiempos quirúrgicos, porque la absorción de la droga en la circulación y la rápida distribución hacia el tejido óseo es buena, a pesar de la gran avidez de la droga el resto de tejido duro circundante. Estudios previos, que usaron alendronato marcado pudieron demostrar que el mismo se absorbe en un 10% a nivel de la cirugía realizada a nivel alveolar. (29)
Si correlacionamos estos efectos a nivel radiográfico, con lo que significó los estudios de citotoxicidad podríamos decir que puede ser una formulación que brindaría beneficios en el lecho óseo bajo estudio. Estudios futuros nos permitirán evaluar los mecanismos de acción a nivel molecular para poder pensar en un futuro en el uso terapéutico clínico en pacientes.
Conclusiones:
Estos estudios preliminares sugieren que el alendronato, colocado en forma parenteral, podría ser efectivo como arsenal terapéutico de gran valor en el tratamiento de la pérdida ósea en patologías de la cavidad oral.
Así mismo se debería evaluar la posibilidad de combinarlo con otros componentes regenerativos tales como: drogas antiinflamatorias, materiales de relleno óseo, técnicas de regeneración tisular guiada, para este tipo de patologías
Bibliografía:
|