Trabajos Originales
El consentimiento informado en las publicaciones de investigación odontológica
Recibido para Arbitraje: 21/10/2014
Aceptado para Publicación: 26/11/2014Ariasgago, O.L., Directora de Proyecto de Investigación - Profesora adjunta de la Cátedra de Odontología Legal, Universidad Nacional del Nordeste, Corrientes, Argentina. Marasso Spaciuk, N.I., Becaria de Investigación, Auxiliar Docente de 1ra. Categoría de la Cátedra de Odontología Legal por concurso, Universidad Nacional del Nordeste, Corrientes, Argentina.
CORRESPONDENCIA: [email protected] - [email protected]
EL CONSENTIMIENTO INFORMADO EN LAS PUBLICACIONES DE INVESTIGACIÓN ODONTOLÓGICA
RESUMEN
Introducción: La investigación odontológica sobre humanos debe seguir los principios de la Bioética. Entre ellos, el de la Autonomía se refleja a través de la implementación del consentimiento informado, instrumento escrito que impide vulnerar el derecho del participante a la elección responsable y a la propia libertad de decisión sobre su cuerpo y su salud. Objetivo: Determinar el tratamiento explícito de los requisitos bioéticos en las publicaciones de investigaciones odontológicas que involucran seres humanos. Metodología: Estudio descriptivo de corte transversal cuya muestra consistió en 100 artículos de investigación en Odontología que involucraban seres humanos. Mediante la aplicación de la prueba estadística Chi cuadrado de Pearson, se analizó la asociación de la variable dependiente Consentimiento Informado con las independientes del estudio (Período, Procedencia, Metodología Empleada, Formato y Disciplina). Resultados: El 68% de los artículos no menciona la realización del consentimiento informado. La relación entre Consentimiento Informado y Metodología arrojó valores estadísticamente significativos, observándose que el 18% de las investigaciones experimentales describían el procedimiento del CI realizado, mientras que en las no experimentales, solo el 5% lo explicaba. La relación con la variable Disciplina reveló un valor p 0,0357, donde el 15% de las publicaciones en el área de investigación clínica detallan en qué consistió el Consentimiento, en el área educación y formación odontológica el 100% no lo mencionan, y en el área de estudios epidemiológicos el 43% lo señala sin describirlo. Conclusión: Los resultados demuestran que los aspectos bioéticos necesarios en toda investigación científica no están evidenciados en las publicaciones odontológicas.
PALABRAS CLAVE: Bioética, consentimiento informado, principio de autonomía
THE INFORMED CONSENT IN DENTAL RESEARCH PUBLICATIONS
ABSTRACT
Introduction: The human dental research should follow the principles of bioethics. Among them, Autonomy is reflected by the implementation of informed consent, written instrument that prevents the violation of the participant right to own responsible choice and freedom to decide on his body and his health. Objective: To determine the explicit treatment of the bioethical requirements of dental research publications involving humans. Methodology: A descriptive cross-sectional study whose sample consisted of 100 research articles in dentistry involving humans. By applying the statistical test of Chi square, it was analyzed the association between dependent variable "informed consent" with the independent variables of the study (Period, Origin, Methodology Employed, Format and Discipline). Results: 68% of the articles did not mention the realization of informed consent. The relationship between Informed Consent and Methodology yielded p value 0.0254, showing that in the 18% of the experimental investigations was explained how it was performed and only in the 5% in non-experimental investigations. The relationship with Discipline variable showed a p value 0.0357, where the 15% of publications in the area of clinical research details the consent performed, in the education and odontological formation area in 100% is not mentioned, and in the area of epidemiological studies in the 43% it was not described. Conclusion: The results demonstrate that the bioethical aspects required in all scientific research are not evidenced in dentistry publications.
KEY WORDS: Bioethics, informed consent, autonomy principle |
La bioética es el área del conocimiento cuya finalidad es ayudar en la reflexión de los conceptos éticos que inciden en las prácticas de las ciencias de la salud.
El gran desarrollo científico de los últimos años en el ámbito de la Odontología precisa el análisis bioético de los métodos científicos aplicados tanto en la generación de conocimiento nuevo como así también en los distintos métodos terapéuticos que las nuevas biotecnologías ofrecen.
En la relación médico/odontólogo paciente, la bioética como disciplina interviene en lo social, en la justicia sanitaria, en la asignación de recursos, investigación, educación para la salud, entre otras áreas, humanizando las profesiones del arte de curar
1.
Las circunstancias históricas de los últimos decenios, determinaron la aparición de numerosas normativas. En 1947 se dicta el Código de Nüremberg
2, que aborda aspectos éticos de la experimentación en seres humanos. La primera disposición del código señala que es esencial el consentimiento informado voluntario del sujeto humano. Otras de las disposiciones que especifica son: la reducción del riesgo y del daño al mínimo, la proporción favorable del beneficio con respecto al riesgo, lo apropiado de los diseños de investigación y la libertad del participante para retirarse en cualquier momento de la investigación
3. El código no trata específicamente la investigación médica en pacientes con enfermedades, pero esta limitación fue tratada en códigos y reglamentos posteriores
4.
En 1964, se promulgó la Declaración de Helsinki, que reconoce el tema de las poblaciones con autonomía disminuida, quienes necesitan de una protección especial. De igual forma, introduce el uso de formularios de consentimiento por escrito donde cada paciente debe plasmar su firma. Esta Declaración ha sido revisada en distintas Asambleas Médicas Mundiales a través del tiempo
5.
Este documento constituyó el cuerpo básico de principios que fueron incorporados desde entonces a las numerosas normas de investigación que han surgido en los diferentes ámbitos de la investigación biomédica
6 e incluyen varios aspectos, entre ellos la necesidad de obtener un consentimiento informado y respetarse la libertad del individuo en cualquier momento del estudio
7.
En 1978, surge el Informe Belmont, cuyo contenido más importante se refiere a los principios éticos fundamentales, y relaciona a cada uno de ellos con los elementos a tener en cuenta en los protocolos de investigación
8.
Los investigadores, las instituciones y, de hecho, la sociedad están obligados a garantizar que estos principios se cumplan y orienten la conducta de quienes participen en la planeación, realización y patrocinio de la investigación con seres humanos
9.
Por tal motivo, surge el documento de consentimiento informado como instrumento escrito que pone de manifiesto las voluntades expresadas, desplegando una nueva relación de tipo contractual: el derecho del paciente a la elección responsable y el respeto a la propia libertad sobre su cuerpo y su salud. El mismo, se basa en el principio de autonomía, el cual es entendido como la capacidad de decisión de las personas así como el derecho a que se respete su voluntad, en aquellas cuestiones que se refieren a ellas mismas. De ahí es que se reconoce la importancia del consentimiento informado como un derecho del paciente y una obligación de los profesionales de la salud en brindarle toda la información necesaria para que a partir de un cabal entendimiento acerca del diagnostico y/o tratamiento, pueda tomar la decisión que él crea más conveniente
10.
En el proceso de obtención del consentimiento informado se debe ofrecer información clara y precisa sobre el objetivo de la investigación, los riesgos y beneficios de la misma, así como las alternativas posibles. Igualmente, se debe informar a los individuos que su participación es voluntaria, que pueden retirarse libremente cuando lo juzguen conveniente, que se guardará confidencialidad de sus datos, que los daños resultantes de la investigación les serán resarcidos y que su negativa a participar en el estudio no afectará sus derechos como paciente
11.
Este proceso juega un papel fundamental en la aplicación de las ciencias de la salud, es por ello que debe ser prestado en forma libre, ser entendible, revelar las características del estudio o intervención, así como también los beneficios y daños de que puedan ocurrir. En caso de que el tratamiento sugerido no fuera aceptado, es necesario dejar constancia de ello. Así quedará en claro tanto el proceso que culmina con la aceptación como la eventual negativa
12.
Queda claro que las investigaciones que se llevan a cabo, con más frecuencia hacen partícipes a los seres humanos y un procedimiento imprescindible en las investigaciones con seres humanos lo constituye el otorgamiento por los sujetos del consentimiento informado para su inclusión en el estudio
13.
La bioética en la investigación pretende que exista una relación creativa y respetuosa donde el investigador realice proyectos válidos, los sujetos estén interesados en participar y la sociedad obtenga resultados que contribuyan a mejorar la calidad de vida del humano
14. La conducta ética del investigador requiere en primer lugar, de la educación en temas de bioética para que crezca el razonamiento moral, el crecimiento de la capacidad para identificar dilemas éticos, de la comprensión o razonamiento de los mismos y del uso de principios éticos reconocidos a fin de encontrar conclusiones que permitan la toma de decisiones moralmente válidas
15. Los fines de la investigación o de la ciencia no pueden prevalecer sobre los del individuo, porque la ciencia está al servicio del hombre y no a la inversa
16.
El objetivo de este trabajo fue determinar el tratamiento explícito de los requisitos bioéticos en las publicaciones de investigaciones odontológicas que involucran seres humanos.
MATERIALES Y MÉTODOSEl presente trabajo es de tipo descriptivo y de corte transversal. La muestra consistió en 100 artículos de investigación en Odontología que involucraban seres humanos correspondientes a formatos on-line (utilizando buscadores virtuales (Latindex y Scielo), e impreso. Este último radicó en artículos de revistas de Odontología disponibles en la Biblioteca de la Facultad de Odontología de la Universidad Nacional del Nordeste.
Los criterios de inclusión que se tuvieron en cuenta fueron: revistas de odontología editadas en castellano, que contengan algún artículo indexado de investigación en humanos, que sea texto completo, empleando un diseño tanto experimental como no experimental, que la edición de la misma ofrezca al menos un ejemplar anual, y que la revista estuviera editada en el período comprendido entre los años 2000 a 2010.
Se encontraron vía online, tres revistas nacionales y siete extranjeras y en formato impreso, cuatro nacionales que cumplían con los mencionados criterios de inclusión.
Para la selección de la muestra se optó por el primer artículo del primer número y volumen de cada año, de cada revista seleccionada de la forma descripta anteriormente.
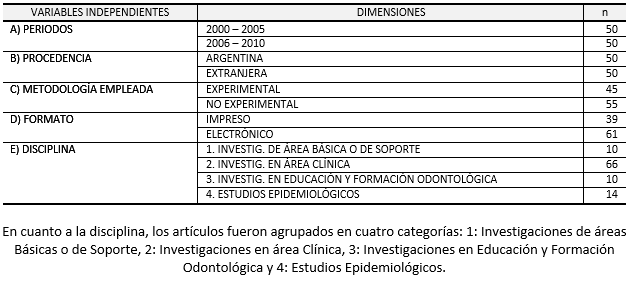
Se armaron grupos como puede observarse en la distribución de la muestra (Tabla I), estableciéndose las siguientes variables independientes: A) Periodo (2000/2005 y 2006/ 2010), B) Procedencia (Argentinas y Extranjeras), C) metodología empleada (Experimental y no experimental), D) Formato y E) disciplinas.
TABLA I
DISTRIBUCIÓN DE LA MUESTRA - VARIABLES INDEPENDIENTES |
 |
|
Para el análisis de la muestra se seleccionaron variables y dimensiones de la siguiente manera:
- Revisión por un comité de ética: A) expresamente menciona que fue evaluado, revisado y aprobado por un comité de Bioética o B) no hace ninguna mención al respecto.
- Consentimiento informado: A) Indica expresamente haberlo realizado y describe detalles acerca del procedimiento efectuado (texto del documento e información verbal que el paciente debe conocer y asentir); B) Sólo menciona que el paciente firmó el consentimiento informado sin puntualizar la manera empleada para llevarlo a cabo; y C) No se menciona el consentimiento informado.
- 3) Justificación del estudio: A) El artículo especifica los beneficios de la investigación y el factor riesgo - beneficio; B) No está explicito, pero se deduce de la lectura del texto; y C) No está explicitado ni describe información orientadora para deducirlo.
- Selección de la muestra: A) Detalla de qué manera se realizó y B) No lo describe.
Además se revisaron las normas de publicación o instrucciones a los autores, respecto de la existencia o no de requisitos éticos.
Para el registro de datos se utilizó una planilla en Excel donde se dispusieron las variables y se efectuó una categorización de las mismas. Mediante la aplicación de la prueba estadística Chi cuadrado de Pearson, se analizó la asociación de la variable dependiente Consentimiento Informado con las independientes del estudio (Período, Procedencia, Metodología Empleada, Formato y Disciplina).
RESULTADOSEn la Tabla II son presentados los valores obtenidos en el total de la muestra. La mayor parte de los artículos (89%) no evidencian haber sido evaluados por un Comité de Bioética y un 68% no menciona la realización del consentimiento informado. Sin embargo en un porcentaje similar (67%) los artículos demuestran haber respetado el principio de Justicia ya que explican en detalle la metodología empleada para seleccionar a los sujetos. Asimismo el 91% de los artículos analizados se explaya sobre la justificación del estudio. Respecto a las normas para autores, en el 67% de las revistas estudiadas no se advierte una normativa expresa respecto a los aspectos bioéticos que deben ser observados para su publicación.
TABLA II
FRECUENCIAS RELATIVAS DE LAS VARIABLES DEPENDIENTES EN LA MUESTRA TOTAL |
 |
|
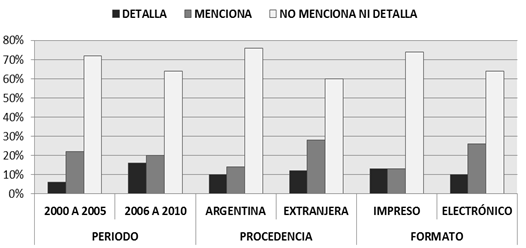
El análisis de la variable Consentimiento Informado mediante la prueba del Chi cuadrado de Pearson, no mostró diferencias estadísticamente significativas al asociarla con las variables "Período", "Procedencia" y "Formato" (gráfico 1).
GRAFICO 1
EL CONSENTIMIENTO INFORMADO: FRECUENCIA RELATIVA DE LA DIMENSIONES |
 |
|
PERÍODO, PROCEDENCIA Y FORMATOEn relación a la variable Período, entre los años 2000 a 2005, el 72% de los artículos no mencionan haber realizado el consentimiento informado (CI) y en el 2º periodo (2006 - 2010), el 64% no citan el CI como parte del proceso de la investigación. En cuanto a la variable Procedencia se observó que en un 76% de las publicaciones de revistas nacionales (Argentinas), no se evidencia la realización del consentimiento informado y en las revistas internacionales, este valor es del 60 %. De igual manera, en la variable Formato se obtuvo un promedio del 69% (entre impresos y electrónicos) de artículos que no mencionan el CI.
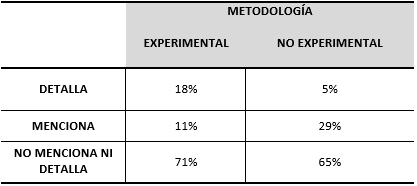
Sin embargo, la aplicación de la prueba del Chi Cuadrado para la asociación entre las variables Consentimiento Informado y Metodología, arrojó valores estadísticamente significativos. El estadístico hallado fue de 7,34 con un p 0,0254, demostrando que ambas variables están relacionadas, observándose que en el 18% de las investigaciones de tipo experimental se explicó minuciosamente de qué manera se llevó a cabo el consentimiento con los sujetos que participaron en el estudio, mientras que en las que emplearon la metodología no experimental, solo el 5% detalló la aplicación del CI. (Tabla III).
TABLA III
EL CONSENTIMIENTO INFORMADO:
FRECUENCIA RELATIVA DE LA DIMENSIÓN METODOLOGÍA |
 |
|
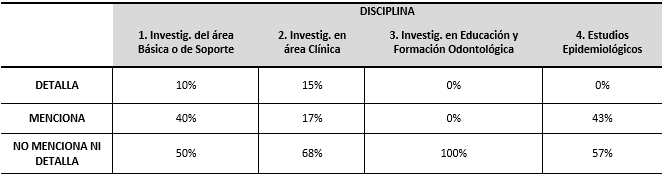
De igual manera, la prueba del Chi Cuadrado para el análisis de la variable Disciplina, reveló una asociación estadísticamente significativa (p 0,0357) entre ambas variables. Puede observarse la tabla IV, que el 15% de las publicaciones en el área de investigación clínica, hace alusión de haber explicado con detalle en qué consistió el CI y el 17% lo menciona, mientras que en el área "Educación y Formación Odontológica" el 100% de los artículos no mencionan ni detallan haber hecho el consentimiento informado a los participantes del estudio y en el área de "Estudios epidemiológicos", el 43% lo señala sin describirlo.
TABLA IV
EL CONSENTIMIENTO INFORMADO:
FRECUENCIA RELATIVA DE LA DIMENSIÓN DISCIPLINA |
 |
|
DISCUSIÓNLa evaluación por un comité de bioética no se evidencia en un gran número de artículos de la muestra. Esta característica está plasmada en la Declaración de Helsinki que aconseja que "…antes de realizar el estudio, el protocolo debe enviarse para consideración, comentario, consejo y aprobación, a un comité de ética de investigación...". Respecto a las normas para autores, en el 67% de las revistas estudiadas no se advierte una normativa expresa respecto a los aspectos bioéticos que deben ser observados para su publicación. Trajano Sardenberg y colaboradores
17 en su trabajo analizando los aspectos éticos referentes a las investigaciones en seres humanos a partir de las Instrucciones a los Autores de revistas científicas brasileñas, demostraron que en el área de odontología, de un total de 44 revistas, el 6,8% presentaron orientaciones éticas.
En este trabajo, los únicos aspectos bioéticos evidenciados en un alto porcentaje de la muestra fueron la variable Selección de la Muestra, demostrando haber respetado el principio de Justicia mediante la explicitación de los criterios utilizados para seleccionar a los participantes de la investigación; y la Justificación del Estudio, a través de una sólida fundamentación para la realización del mismo.
Analizando la variable Consentimiento Informado en el total de la muestra, sólo el 32% de los trabajos revisados expresan haber realizado el Consentimiento Informado, explicando con detalles la manera que se utilizó para llevar adelante el proceso del consentimiento y en otros casos sólo mencionándolo sin dar precisiones, es decir de aquellos recaudos y procedimientos por el cual se explica al individuo que participa en una investigación sobre todos los aspectos de la misma, como la metodología en la cual va a ser sometido, beneficios, riesgos, tratamientos alternativos, etc., invitándolo a firmar su aceptación a formar parte de la investigación una vez recibida y comprendida toda la información suministrada.
Esta variable fue utilizada para el análisis de los aspectos bioéticos, debido a que es una recomendación clave y fundamental en la protección de las personas preconizados en los documentos de Bioética. Así, la Declaración de Helsinki expresa "…y cada uno de estos debe recibir información adecuada sobre objetivos, métodos, financiamiento, afiliaciones institucionales, beneficios calculados, riesgos previsibles y todo aspecto pertinente de la investigación. Luego de lo cual debe prestar el consentimiento informado…".
En su mayoría los artículos que no mencionan ni detallan la realización del consentimiento informado son aquellos que utilizan una metodología de tipo no experimental. El 100% de los trabajos revisados en el área "Educación y Formación Odontológica" (disciplina categorizada en este trabajo como área 3), no mencionan haber aplicado el consentimiento informado, dato coincidente con la metodología no experimental, ya que en la muestra (por azar) de ésta área, quedó incluido el 80% de trabajos con este diseño (no experimental). De acuerdo al la investigación de Mancini Rueda y Lolas Stepke18, cuyo objetivo general fue determinar el cumplimiento explícito de requisitos bioéticos básicos en estudios científicos en seres humanos, indexados en las bases bibliográficas LILACS y MEDLINE, hallaron que el 68% de los artículos de metodología no experimental no señalan haber realizado consentimiento informado y el 51% de los estudios experimentales tampoco lo mencionan.
Cabe acotar que la Organización Panamericana señala que "…En varios tipos de investigaciones epidemiológicas, el consentimiento informado personal es impracticable o no es aconsejable. En esos casos, la comisión de evaluación ética debe determinar si es éticamente aceptable proceder sin el consentimiento informado individual, y si los planes del investigador para salvaguardar la seguridad de los sujetos, respetan su derecho a la intimidad y mantienen el carácter confidencial de los datos son apropiados..."
19.
De todas maneras se rescata que es el Comité de Bioética, el que deberá expedirse acerca de la implementación o no del Consentimiento como así también asegurarse que el derecho a la intimidad y la confidencialidad de los participantes sean respetados.
La muestra total demuestra que los aspectos bioéticos necesarios en toda investigación científica, no están evidenciados en las publicaciones.
Los resultados de este estudio no demuestran que los aspectos éticos no fueron tenidos en cuenta, sino que analizan el fenómeno de la exteriorización de los mismos en la publicación.
Cabe aclarar que los resultados de este estudio no son indicadores de falta de recaudos éticos en la investigación científica odontológica, sino que analiza el fenómeno de la exteriorización de los mismos en la publicación.
En la investigación odontológica, se observa que si bien el Código de Ética puntualiza los aspectos bioéticos a tenerse en cuenta como así también las pautas, sugerencia y consejos establecidos en los documentos que fueron descriptos arriba, no se observa que estén reflejados en los trabajos difundidos, como así también en muchos casos no están comprendidas en las políticas editoriales de las revistas.
Creemos que los requerimientos bioéticos, tal cual están expresados en los documentos, deberían estar incluidos en el texto del artículo, por tal motivo este trabajo tiende a reflexionar sobre la necesidad de explicitar los aspectos bioéticos en toda investigación en seres humanos, para que sea fuertemente interiorizada por la comunidad científica que los consulta.
REFERENCIAS BIBLIOGRÁFICAS
- Guerra Rina Ana. Bioética en la malla curricular de Odontología. Acta bioeth. [revista en la Internet]. 2006, obtenible en: < http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S1726-569X2006000100007&lng=es. doi: 10.4067/S1726-569X2006000100007> [consulta 20 junio 2011]
- Bunge, M. Ética y Ciencia. 3ra. ed. Buenos Aires. Siglo XX. 1983.
- Calva Rodríguez, R.: Bioética. México D.F. Ed. McGraw Hill. 2006.
- Código de Nüremberg. Tribunal Internacional de Nuremberg, 1947. Traducción adaptada de Mainetti, J.A. Ética médica. La Plata, Argentina. Ed. Quirón. 1989.
- Declaración de Helsinki de la Asociación Médica Mundial. Principios éticos para las investigaciones médicas en seres humanos. 52 Asamblea General Edimburgo, Escocia, 2000. En: http://www.csjn.gov.ar/cmf/hel.html
- Herranz, G. Experimentación científica en el hombre. Capítulo 17 de Deontología Biológica. En: <http://www.unav.es/cdb/dbcapo17a.html>
- Olivero, Rosa; Domínguez Antonio; Malpica Carmen Cecilia. Principios bioéticos aplicados a la investigación epidemiológica. Acta bioeth. 2008, obtenible en: <http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S1726569X2008000100012&lng=es. doi: 10.4067/S1726-569X2008000100012> [consulta: 10 Septiembre 2010]
- El Informe Belmont. Principios y Guías Éticos para la protección de los sujetos humanos de investigación. En: http://www.bioeticas.org/bio.php?articulo62
- Sánchez, M.: Historia, Teoría y método de la medicina: introducción al pensamiento médico. Barcelona. Editorial Masson S.A. 1998.
- Islas-Saucillo M y Muñoz CH. El consentimiento informado. Aspectos Bioéticos. Rev Med Hosp Gen Mex 2000; 63 (4): 267-273.
- Mfutso-Bengo J, Masiye F, Muula A. Ethical challenges in conducting research in humanitarian crisis situations. Malawi Med J 2008; 20(2): 46-49.
- Manrique JL, Cottely E, Rossi RP, Smith R. Consentimiento informado: fundamento ético, médico y legal. Rev Argent Cirug 1991; 61: 99-102.
- Declaración de Helsinki de la Asociación Médica Mundial. Principios éticos para las investigaciones médicas en seres humanos. 52ª Asamblea General de Edimburgo, Escocia, octubre del 2000.
- Martínez-Otero Pérez V.: Temas de nuestro tiempo, Psicología, educación, Sociedad y Calidad de Vida. Madrid. Ed. Fundamentos. 1999.
- Breña Sánchez J., Breña Sánchez G., Breña Sánchez R.: Ética y valores 1. México. Ed. Esfinge. 2005.
- Taylor S, Bogdan R.: Introducción a los métodos cualitativos de investigación social: la búsqueda de significados. Madrid. Ed. Paidós. 1992.
- Sardenberg Trajano, Müller SS, Pereira Hamilton R, Oliveira RA, Hossne William S. ANÁLISIS DE LOS ASPECTOS ÉTICOS DE LA INVESTIGACIÓN EN SERES HUMANOS CONTENIDOS EN LAS INSTRUCCIONES A LOS AUTORES DE 139 REVISTAS CIENTÍFICAS BRASILEÑAS. Acta bioeth. 2000, obtenible en: <http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S1726-569X2000000200008&lng=es. doi: 10.4067/S1726-569X2000000200008> [consulta: 2 Septiembre 2010]
- Mancini Rueda Roberto, Lolas Stepke Fernando. EVALUACIÓN BIOÉTICA DE TRABAJOS DE INVESTIGACIÓN EN SERES HUMANOS PUBLICADOS EN AMÉRICA LATINA Y EL CARIBE. Acta bioeth. 2001, obtenible en: <http://www.scielo.cl/scielo.php?pid=S1726-569X2001000100012&script=sci_arttext> [consulta: 21 Marzo 2012]
- Normas Éticas del PSI para investigaciones con sujetos humanos. Obtenible en Organización Panamericana de la Salud - Oficina Regional de la Organización Mundial de la Salud (OPS/OMS):http://medicina.uc.cl/docman/368/doc-download [consulta: 14 Agosto 2013]
|




