Revisiones Bibliográficas
Terapia láser de baja intensidad Tlbi con láser ER:YAG y ND:YAG como alternativa en el tratamiento de la Osteonecrosis inducida por Bifosfonatos en el maxilar y mandíbula
Recibido para Arbitraje: 20/05/2014
Aceptado para Publicación. 29/11/2014Pardiña P., Egresado de La Facultad de Odontología Universidad Rómulo Gallegos 2012. Miembro activo ASOVAC capítulo Aragua.
CORRESPONDENCIA: [email protected]
TERAPIA LÁSER DE BAJA INTENSIDAD TLBI CON LÁSER ER:YAG Y ND:YAG COMO ALTERNATIVA EN EL TRATAMIENTO DE LA OSTEONECROSIS INDUCIDA POR BIFOSFONATOS EN EL MAXILAR Y MANDÍBULA
RESUMEN
La osteonecrosis en el maxilar o mandíbula amerita un tratamiento inmediato para interrumpir el avance de la enfermedad, siendo la Terapia Láser de Baja Intensidad (TLBI) una alternativa favorable en su tratamiento. Introducción. Los bifosfonatos son análogos sintéticos, que inhiben la actividad osteoclástica en el tejido óseo. Sin embargo, son causantes de osteonecrosis en el maxilar y mandíbula. Así mismo, dicha patología puede aparecer de forma espontánea o ser desencadena luego de cualquier proceso quirúrgico o injuria externa en la cavidad bucal. El tratamiento está basado en métodos convencionales no quirúrgicos y quirúrgicos. Sin embargo, Existe un número considerable de pacientes que padecen de osteonecrosis, que no responden a los tratamientos expuestos; esto impulsa la búsqueda de nuevas tendencias que solas o junto a los protocolos de atención ya establecidos, mejoren a los pacientes o erradiquen el cuadro clínico en su totalidad. Objetivos. Puntualizar las características de la Terapia Láser de Baja Intensidad con láser Er:YAG y Nd:YAG y los beneficios de su uso sobre la osteonecrosis inducida por bifosfonatos en el maxilar o mandíbula. Conclusiones. El estudio documental arrojo como resultado que la TLBI en combinación con la antibiótico terapia, puede ser considerado una alternativa viable en el tratamiento de la osteonecrosis inducida por bifosfonatos; debido a que al descontaminar y bioestimular la zona bucal afectada en la que es aplicado, acelera la regeneración del tejido óseo y blando.
PALABRAS CLAVE. Bifosfonatos, osteonecrosis, Láser Er:YAG, Láser Nd:YAG.
LOW LEVEL LASER THERAPY LLLT WITH LASER ER:YAG AND ND: YAG AS ANALTERNATIVE IN THE TREATMENT OF OSTEONECROSIS INDUCED BY BIPHOSPHONATE IN THE MAXILLA AND MANDIBLE
ABSTRACT
Osteonecrosis in the maxilla or mandible warrants an immediate interrupt the progression of the disease treatment, with the Low Intensity Laser Therapy ( LLLT ) treatment in a favorable alternative. Introduction. Bisphosphonates are synthetic analogs which inhibit osteoclast activity in bone tissue . However, they are the cause of osteonecrosis in the maxilla and mandible. Also, this disease can appear spontaneously or be triggered after any surgical procedure or external injury in the oral cavity. The treatment is based on conventional non -surgical and surgical methods. However, there a considerable number of patients suffering from osteonecrosis , which do not respond to treatments exposed ; this drives the search for new trends alone or together with established treatment protocols , patients improve or eradicate the clinical picture as a whole. Objectives. To clarify the characteristics of Low Intensity Laser Therapy laser Er: YAG and Nd : YAG and benefits of the use of bisphosphonate -induced osteonecrosis in the maxilla or mandible. Conclusions . The desk study results throw that LLLT in combination with antibiotic therapy, can be considered a viable alternative in the treatment of bisphosphonate -induced osteonecrosis ; because when decontaminating and oral bioestimular affected area in which it is applied, accelerates the regeneration of bone and soft tissue
KEY WORDS: Bisphosphonates , osteonecrosis , Er: YAG, Nd: YAG. |
El remodelado óseo constituye un proceso biológico complejo, que ocurre durante toda la vida, pero solo hasta la tercera década el balance es positivo. Es precisamente a partir de los treinta años que existe la máxima masa ósea, que se mantiene con pequeñas variaciones hasta los 50 años; a partir de aquí, existe un predominio de la resorción y la masa ósea comienza a disminuir. Tanto por efectos de la edad, como por alteraciones en las condiciones sistémicas del individuo. Muchos pacientes pueden desarrollar patologías óseas que debilitan los huesos entre las que se pueden mencionar osteogénesis imperfecta, mieloma múltiple, enfermedad de Paget, osteoporosis y metástasis óseas. En estas entidades el hueso es debilitado, por lo que puede fracturarse o lesionarse incluso ante presiones mínimas. En función de detener y curar dichas manifestaciones patológicas, los laboratorios farmacéuticos han diseñado un grupo de medicamentos llamados bifosfonatos, cuyo uso comenzó de forma industrial en la década de 1960, cuando fueron sintetizados por químicos alemanes. A pesar de las ventajas que se han obtenido con los bifosfonatos, numerosos estudios han reportado la aparición de osteonecrosis de los maxilares en pacientes que reciben terapia con estos medicamentos
1. En 2003 y 2004 se publicaron los primeros casos de esta patología en pacientes que recibieron dosis muy altas de bifosfonatos, en un contexto de enfermedad neoplásica con metástasis, siendo muy escasos los casos descritos entre los pacientes que reciben fármacos a dosis para enfermedades como osteoporosis. Aun así, se genero una alarma en la comunidad científica como de la población en general
2. Las formas actuales de tratamiento para a ONM inducida por bifosfonatos son controvertidos y su uso sigue siendo una problemática. Hay directrices que basadas en la evidencia que los pacientes experimentan mejoría de los síntomas después del uso de antibióticos por vía oral. Sin embargo, a menudo requieren su uso de forma prolongada o administrarlos por vía intravenosa. El objetivo de cada tratamiento se enfoca en aliviar el dolor reducir la infección y estabilizar la progresión de la enfermedad. Diferente a estas terapias que en algunos casos resultan poco exitosas, se buscan nuevos protocolos de tratamiento para la ONM; siendo la terapia mínimamente invasiva con láseres una opción viable aplicada en los últimos 5 años
3.
REVISIÓN DE LA LITERATURABIFOSFONATOSFueron compuestos sintetizados por primera vez en el siglo XIX, con propósitos industriales como agente anti - sedimentación y para prevenir la formación de carbonato de calcio. En 1969, fué publicado por primera vez sobre los bifosfonatos en el Sciencie and Nature; lo que permitió que 20 años más tarde por sus características biológicas fueran utilizados como drogas para las disfunciones oseas4. Dichos compuestos, son análogos del pirofosfato que se caracterizan por la presencia de dos átomos de fosforo unidos a un átomo de carbono, lo que les confiere una gran resistencia a la hidrólisis enzimática y les permite unirse fuertemente a la hidroxiapatita de la matriz mineralizada. En la actualidad, patologías como osteoporosis, enfermedad de Paget, osteogénesis imperfecta, lesiones osteolíticas asociadas a metástasis óseas o al mieloma múltiple y la hipercalcemia maligna son tratadas con los bifosfonatos5.
MECANISMO DE ACCIÓNSu mecanismo de acción consiste en inhibir la actividad osteoclástica en el tejido óseo. Cuando comienza el proceso de resorción del hueso que está impregnado de bifosfonato, este es liberado y captado por el osteoclasto, deteriorando su capacidad de adherirse a la superficie del hueso y de producir los protones y enzimas lisosómicas necesarias para continuar la resorción ósea. Algunos bifosfonatos interfieren con la activación y diferenciación de células precursoras esteoclásticas en osteoclastos maduros, con la quimiotaxis y su adherencia al hueso culminando con la reducción del número de osteoclastos, al inducir la apoptosis de estas células por lo que tienen potencial antitumoral. Los bifosfonatos también pueden actuar indirectamente estimulando la formación de precursores de los osteoblastos, incrementando el número, diferenciación y permitiendo que estas células liberen sustancias que inhiban a los osteoclastos
1.
Dichos medicamentos a su vez pueden administrarse por vía oral o intravenosa siendo los segundos los que ejercen su efecto más rápido en el organismo. Los mismos tienen la particularidad de depositarse en el hueso y se mantenerse en él durante un periodo de 10 años en el caso del acido zoledrónico, el acúmulo de estos va depender de la dosis administrada y el tiempo de uso y la vía utilizada
1,5. (Tabla I)
Tabla I
Características farmacológicas diferenciales de bifosfonatos orales e intravenosos1 |
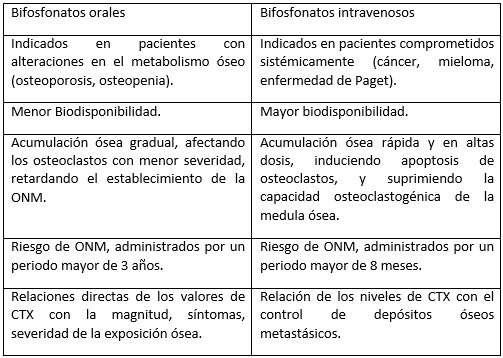 |
| Fuente: Osteonecrosis de los maxilares inducida por bifosfonatos.pag. 49 |
Los bifosfonatos por vía oral más usados son
6- Alendronato (Fosamax®)
- Clodronato (Bonefos®)
- Etidronato (Difosfen®, Osteum®)
- Risedronato (Actonel®, Acrel®)
- Tiludronato(Skelid®)
Los bifosfonatos más usados por vía parenteral son6
- Ácido Ibandrónico o Ibandronato (Bondronat®), Bondeza®)
- Pamidronato (Aredia®, Linoten®, Xinsidona®)
- Zoledronato (Zometa®)
Los bifosfonatos se unen preferiblemente a los huesos con recambio óseo más alto, teniendo mayor afinidad por el hueso trabecular. Los huesos maxilares, a diferencia de otros tejidos óseos del organismo poseen un gran aporte sanguíneo y una mayor velocidad de recambio óseo. Debido a la presencia de estructuras dentales que continuamente están ejerciendo estímulos mecánicos lo cual genera una demanda continua de remodelado óseo alrededor del ligamento periodontal. Es por esto, que los bifosfonatos se concentran en un gran porcentaje en los huesos maxilares Esta consideración aunada a procesos crónicos invasivos, tratamientos quirúrgicos, biotipo delgado de mucosa en ciertas regiones de la cavidad oral, hacen susceptible al tejido óseo padecer de osteonecrosis al recibir tratamiento odontológico de tipo quirúrgico invasivo
1.
EFECTOS ADVERSOSSe han descrito diferentes efectos adversos y complicaciones asociadas a su uso. En el caso de los bifosfonatos orales, los efectos secundarios más frecuentes son: erosiones orales, úlceras gástricas, esofagitis y estenosis esofágica. Entre los efectos adversos de los bifosfonatos intravenosos si su infusión es rápida, está la insuficiencia renal. Además, se han descrito flebitis, febrícula transitoria, escalofríos, síndrome pseudogripal en los dos primeros días. Especial relevancia ha adquirido durante los últimos años la aparición de numerosos casos de osteonecrosis avascular inducida por bifosfonatos en pacientes en tratamiento con bifosfonatos. La Osteonecrosis Avascular de los maxilares se ha convertido en los últimos años en una patología frecuente e importante en pacientes con diferentes patologías sistémicas óseas que están en tratamiento con bisfosfonatos.
6OSTEONECROSIS DE LOS MAXILARES (ONM)Con objeto de diferenciar la ONM de otras enfermedades que cursan con exposición ósea y retrasos en la cicatrización de los procesos alveolares, la Sociedad Americana para la Investigación Ósea y Mineral establece 3 características que los pacientes deben cumplir: 1- Tratamiento actual o previo con bifosfonatos. 2- Hueso necrótico expuesto en la región maxilofacial que persiste más de 8 semanas. 3- No antecedentes de radioterapia en la región maxilofacial
5. Sin embargo, otros autores difieren en el hecho de que pueden haber la presencia de una o varias lesiones ulceradas en la mucosa de los procesos alveolares, con o sin exposición o del hueso mandibular o maxilar, pero con dolor o fístulas que deben ser considerados como candidatos para llevar a cabo estudios más detallados
2. Es decir, que la lesión puede presentarse tras una extracción dental o de forma espontanea. A su vez, las entidades que deben considerarse dentro del diagnóstico diferencial son: osteítis alveolar, sinusitis, gingivitis y periodontitis, caries, enfermedad periapical y alteraciones de la articulación temporomandibular
5.
FISIOPATOLOGÍALa inhibición de la remodelación ósea es el mecanismo principal asociado a la ONM. Los bifosfonatos alteran de manera específica la función de los osteoclastos y reducen su número, en parte al inducir la apoptosis en ellos. Pruebas obtenidas recientemente sugieren que los bifosfonatos que contienen nitrógeno, inhiben también la prenilación de las proteínas, que constituyen uno de los productos terminales de la vía del acido melavolónico. Este efecto transtorna el tráfico intracelular de las proteínas y puede tener como resultado final la apoptosis
7.
Así mismo, se plantea una hipótesis, en cuanto a la inhibición de la formación de vasos sanguíneos por parte de los bifosfonatos, como parte responsable del desarrollo de ONM. Se ha demostrado que la terapia con bifosfonatos retrasa la cicatrización de las heridas posterior a la extracción de piezas dentales, esto por la inhibición de la angiogénesis in vivo. Sin embargo, se desconoce si su efecto anti angiogénico es por la inhibición de la vía osteoclástica o de otras células. Es importante destacar que a pesar de que frecuentemente se utiliza el término necrosis avascular para describir la ONM, no existe evidencia de que haya reducción de la vasculatura o del suplemento sanguíneo
7.
Otro punto que debe tomarse en cuenta, es los cientos de microorganismos que existen en la cavidad bucal, lo que evidentemente aumenta el riesgo de infección posterior a un procedimiento dental; esto aunado a que la mayoría de los pacientes con cáncer son tratados con inmunosupresores. Todos estos factores, junto con la mala higiene bucal, exponen el hueso a la flora, que se infecta produciendo dolor, inflamación, infección con supuración y finalmente, necrosis ósea
7.
ESTADIOS DE LA ONMLa ONM se manifiesta clínicamente como una exposición ósea (hueso blanco de color amarillento) en la cavidad oral. Al principio, es asintomático, pero se convierte en sintomática cuando se genera una infección secundaria por un traumatismo en el tejido blando subyacente. Pueden producirse pérdidas de piezas dentales, inflamación de tejidos blandos, fistulas, dolor, disestesias, abscesos dentales, etc. Los síntomas pueden aparecer espontáneamente en el hueso o más frecuentemente, en el sitio de una extracción dental previa
5.
En el 2009 la AAOMS establece la clasificación de los estadios clínicos de la ONM entre los cuales se destacan:
Categoría de riesgo: no aparente necrosis ósea en pacientes que han sido tratados con bifosfonatos VO o IV.
Estadio 0: no hay evidencia clínica de necrosis ósea. Pero hallazgos clínicos y físicos inespecíficos.
Estadio I: exposición y necrosis ósea, asintomáticos y sin evidencia de infección.
Estadio II: exposición y necrosis ósea. Infección (dolor, eritema con/sin drenaje purulento).
Estadio III: exposición y necrosis ósea con dolor e infección y uno o más de los siguientes: exposición y necrosis ósea, que se extiende más allá de la región alveolar del hueso (borde inferior y rama de la mandíbula, seno maxilar y cigoma en la maxila) resultando en fractura patológica, fístula extra-oral, comunicación antral oral/nasal oral, y ostiólisis que se extiende al borde inferior de la mandíbula
7.
PRUEBAS COMPLEMENTARIASLa más utilizada la ortopantomografía, que en estadios precoces no aporta información. Posteriormente se ven áreas radiolúcidas y radiopacas, relacionadas con secuestros óseos e incluso destrucción ósea (osteólisis).La tomografía computarizada y la resonancia magnética permiten un diagnóstico precoz y establecen la verdadera extensión de la osteonecrosis (estadio clínico). Se recomienda la realización de cultivos microbiológicos y antibiogramas. La biopsia ósea solo se hará si se sospecha que la lesión guarda relación directa con la enfermedad (neoplasia) que motivo la utilización iv de los bifosfonatos. La determinación sérica del telopéptido c-terminal del colágeno tipo I (ctx) no es predictiva del desarrollo de ONM a nivel individual, pero puede identificar a aquellos pacientes que se encuentran en zona de riesgo: Si ctx < 100 pg/ml = riesgo alto. Si ctx entre 100 y 150 pg/ml = riesgo moderado. Si ctx > 150 pg/ml = riesgo bajo
5.
TRATAMIENTOLas pautas generales para el tratamiento de la ONM son: higiene oral y colutorios con clorhexidina 0,12 % sumado al tratamiento antibiótico de forma continua o intermitente y evitar cirugía o desbridamiento amplio en la medida de lo posible. Se deben evitar los procedimientos quirúrgicos dentoalveolares electivos e los pacientes con ONM establecida, porque el área quirúrgica puede llevar a una nueva área de hueso necrótico expuesto
8.
PLAN DE TRATAMIENTO ESTIPULADO POR ESTADIOSEstadio I - se recomienda enjuagues con solución de clorhexidina al 0,12 % o al 0.2 %, 3 veces por día, o topicaciones con gel de clorhexidina a las que se puede ayudar con placas de protección.
Estadio II - Además de los cuidados locales con clorhexidina gel o solución, se agrega el uso de AINES y antibioterapia para evitar la infección, que es una de las causas de progresión de la lesión.
Amoxicilina/clavulánico 875/125 mg cada 8 horas, por un período de 15 días.
En casos de alergia clindamicina 300 mg cada 6 horas, levofloxacino 500 mg cada 24 horas, metronidazol 500 mg cada 8 horas, doxiciclina 100 mg cada 24 horas ó azitromicina 500 mg cada 24 horas.
Estas pautas son variables y según la evolución de la lesión, se describen combinaciones de antibióticos.
Si se sospecha de la posibilidad de una micosis, se dispone de la nistatina, miconazol o del fluconazol.
Estadio III - Se recomienda utilizar antibióticos de forma I/V. Los cultivos microbiológicos no son de utilidad, por la contaminación superficial habitual de la flora oral (biofilm). El tipo de tratamiento quirúrgico y el momento de realizarlo es quizás donde más dudas se plantean. La mayoría de los autores son partidarios de un tratamiento conservador, evitando desbridamientos agresivos debido a las recidivas y a las secuelas posteriores, corriendo el riesgo de aumentar el tamaño de la lesión. Se han utilizado desde técnicas basadas en el legrado y/o extirpación de fragmentos móviles y técnicas más agresivas que integran secuestrectomías y extirpaciones marginales o segmentarias. Si el hueso expuesto exhibe movilidad o evidencia radiográfica de secuestro, entonces debe ser eliminado. Los partidarios de tratamientos quirúrgicos agresivos prefieren desbridar ampliamente la zona y hacer un cierre primario, separando así la lesión de la flora oral, intentando evitar las infecciones crónicas y asociando en ocasiones técnicas de reconstrucción
8.
PAUTAS DE TRATAMIENTO PARA LOS PACIENTES QUE CONSUMEN LOS BIFOSFONATOS POR VÍA PARENTERALLa variante fundamental en éstos pacientes, es la dosis y la rápida y alta biodisponibilidad del fármaco, esto hace que los tiempos establecidos de 3 años para quienes se les administra por vía oral, se acortan a 8 meses. Por lo que se hace estricto el rápido protocolo odontológico preventivo previo a iniciar su administración
8.
Es preciso señalar que, las formas actuales de tratamiento para la osteonecrosis inducida por bifosfonatos son controvertidos. Hay directrices basadas en la evidencia sobre la ONM que informan buenos resultados durante un largo plazo de seguimiento. Los pacientes experimentan una mejoría de los síntomas después del uso de antibióticos por vía oral en combinación con enjuagues de clorhexidina al o,12%. Sin embargo, a veces estos protocolos requieren del uso de antibioticoterapia por vía endovenosa o el mantenimiento por vía oral por largos periodos de tiempo. El objetivo del tratamiento se enfoca en aliviar el dolor reducir la infección y estabilizar la progresión de la enfermedad. Debido a estos resultados, se buscan nuevas estrategias para propiciar una resolución de la ONM que permita obtener resultados más certeros. En los últimos 5 años se ha empleado la terapia con láseres bioestimulantes como estrategias invasivas para tratar la ONM
3.
Como siempre, una buena historia clínica nos alertará de la posible situación de riesgo del paciente, en este caso asociado a la toma de un fármaco. El mejor tratamiento consiste en la prevención de los posibles riesgos.
6Ante cualquier intervención quirúrgica a nivel bucal, es importante informar al paciente del riesgo inherente a la medicación que toma o ha tomado y acreditarlo mediante la firma del consentimiento informado. Los pacientes deberán conocer que si están tomando bifosfonatos por vía oral, el riesgo de osteonecrosis es menor que si los recibieran por vía intravenosa. También deberán saber que el riesgo es proporcional al tiempo que llevan recibiendo el tratamiento y que para disminuir este riesgo es muy importante mantener una buena higiene bucal, no tener hábitos nocivos y realizar controles odontológicos periódicos. Deberán conocer que en la actualidad, no existe ninguna técnica que determine de forma eficaz el riesgo de cada paciente. Y deberán tener presente que ante la menor sensación de molestia o ante una lesión ósea en la boca deberán acudir inmediatamente a su odontólogo, puesto que el tratamiento precoz, mejora sensiblemente la evolución de estas lesiones.
6LÁSER ER:YAGTiene como medio activo un cristal de itrio-aluminio-granate al que va añadido erbio. Su longitud de onda es de 2,94nanometros, y se aplica mediante fibra óptica en pulsos. Tiene una gran adsorción por el agua y la hidroxiapatita, por lo que se ha empleado en el tratamiento de caries y preparación de cavidades en los dientes (el mayor contenido en agua de la caries respecto al tejido dental sano permite que el láser actue preferiblemente sobre ella). Su efecto sobre la hidroxiapatita no es fototérmico sino fotomecánico, la expansión brusca de volumen de agua en el interior del tejido duro dental produce una explosión del tejido debido al aumento de presión mecanismo conocido como ablasión. Por ello, este láser se utiliza con un pulverizador de agua que potencia su efecto. Su capacidad hemostática es limitada, lo cual limita también su utilización en el resto de la cirugía bucal
9.
Por otro lado, los pulsos que emite este láser producen un corte de hueso con un mínimo daño térmico permitiendo además que el corte sea muy preciso. Esto se debe al mecanismo antes explicado que hace posible la ablasión del tejido incidiendo únicamente a nivel superficial no generando daños térmicos subyacentes. Se ha demostrado que el hueso tendrá una curación más rápida, así como una mayor osteoinducción
10. A su vez el láser ER:YAG es capaz de destruir las bacterias al provocar la evaporación de su líquido intracelular, esta capacidad de esterilizar las superficies sobre la que se incide es una de las principales ventajas para su utilización en odontología. Un estudio hecho por la facultad de odontología de la universidad de Complutense de Madrid en el 2006; demostró el efecto esterilizante de dicho láser al aplicarlo con distintas intensidades sobre dientes in vitro
11.
LÁSER Nd:YAGSu medio activo es un cristal de itrio-aluminio-granate, cargado con iones de neodimio, y se aplica mediante fibra óptica, generalmente en modo de contacto. Su longitud de onda es de 1,06 nanómetros, en la parte del espectro infrarrojo cercano. Se adsorbe por el agua y el tejido pigmentado al tener afinidad por la melanina con una gran penetración, permitiendo una coagulación en profundidad (puede sellar vasos de hasta 2-3mm de diámetro). Su adsorción por el tejido duro dental es escasa, por lo que puede emplearse en el tratamiento de la enfermedad periodontal y sobre tejidos blandos de forma segura
9.
El láser Nd:YAG, fué utilizado inicialmente para el tratamiento de la caries. Pero como resultado de numerosos estudios e investigaciones; con el paso del tiempo su uso se ha limitado básicamente, a los tejidos blandos gracias a su poder descontaminante. Las ventajas que ofrece este láser son: una intervención quirúrgica desarrollada en un campo limpio y libre de microorganismos y, que se pueden llevar a cabo incisiones nítidas que requiere menor cantidad de anestésico local. Generalmente no es necesario suturar, debido a que los postoperatorios cursan normalmente casi sin dolor ni edema; la cicatrización es rápida y sin evidencias de recidiva cuando se efectúa la exéresis de lesiones proliferativas
12.
Existen técnicas fototérmicas básicas, para la utilización de este láser en los tejidos blandos del área bucofacial: incisión y excisión, ablasión o vaporización y hemostasia. Una vez elegida la técnica que se desea emplear, es necesario controlar los parámetros del láser en lo que se refiere a: la potencia y el tiempo para conseguir el objetivo deseado, con un mínimo daño colateral
12.
TERAPIA LÁSER DE BAJA INTENSIDAD EN LA ONMNecrosis ósea avascular, colonias de bacterias y hongos, así como abundante infiltración inflamatoria se observan con frecuencia en la ONM. Los bifosfonatos inhiben la capacidad de reparación del hueso después de microdaños. Además, estos fármacos disminuyen la proliferación de células epiteliales a través de la reducción de los Farnesil difosfato sintetasa y exiben propiedades anti-angiogénicas, incluyendo la inhibición del factor de crecimiento endotelial vascular. La alteración de la angiogénesis, puede tener efectos importantes en la calidad y la cantidad de la vascularización del hueso, posiblemente alterar la respuesta al trauma e infecciones
3.
Varios estudios, han demostrado los efectos positivos de la terapia láser de baja intensidad (TLBI), con diferentes longitudes de onda en el proceso de curación de una amplia gama de trastornos de mucosa, ósea, y cutánea. Estas observaciones, apoyan la posible validez de bioestimulación láser en el tratamiento de la ONM. Como se ha informado en la literatura, las longitudes de onda de láser con efectos bioestimulantes en el área maxilofacial son argón, CO
2, He-neón, Er: YAG, Diodo, Nd: YAG y KTP
3.
El haz de láser produce varios cambios en el metabolismo celular. Particularmente, la luz es absorbida por los foto aceptantes primarios, lo que dispara los mecanismos de regulación de las células. La intensidad de los efectos se basa en el estado fisiológico de las células durante la irradiación y en la longitud de onda aplicada. La eficacia de la TLBI implica probablemente un mecanismo fotoquímico con foto-energía, siendo adsorbida por los fotocromos mitocondriales intracelulares y luego se convierte a energía metabólica. Haciendo de esta forma la cadena respiratoria citocromo. La luz del láser provoca una acumulación de oxigeno atómico, el cual actúa como un radical libre y por lo tanto altera la producción de ATP y la formación de gradientes de protones transmembrana electroquímicas en las mitocondrias. La irradiación parece aumentar la liberación de prostaglandina E2 (PGE2), que contribuye a la sanación de hueso y mucosa
3.
Un mecanismo de dos pasos está implicado en la interacción entre la irradiación y la reparación ósea: (1) la activación de los osteoblastos para producir matriz ósea y (2) un inhibidor fotobiológico que resulta en la disminución de la actividad osteoblástica. Además, la TLBI estimula la actividad de los osteoclastos para promover la resorción y remodelación del hueso. Efectos estimulantes sobre la formación ósea, han sido obtenidos por irradiación repetida con una dosis baja de energía durante un periodo de tiempo, que por una única irradiación con la misma dosis total de energía. La curación de los tejidos blandos también se mejora con la TLBI. En particular, existe un acortamiento de la fase de exudación y una estimulación de los procesos de reparación, promoviendo así la formación de tejido de granulación. La transformación de fibroblastos en miofibroblastos puede acelerar la curación de la piel y la mucosa. Esto es de particular relevancia en las condiciones de la necrosis avascular de la ONM, donde es muy importante estimular la vascularización y el tropismo de los tejidos blandos
3. (Figura 1)
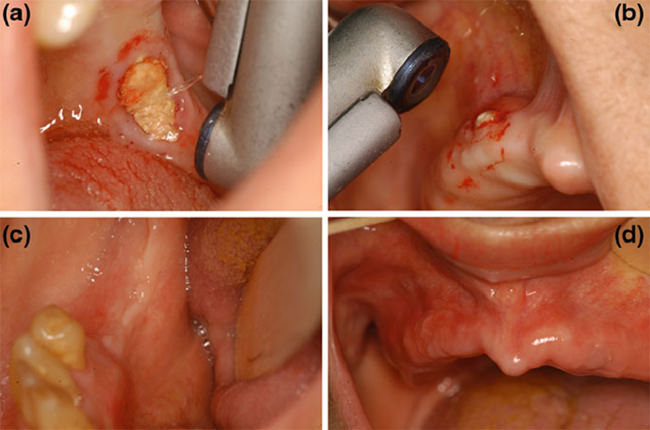 |
Figura 1
a- Vaporización del hueso necrótico mandibular con láser ER:YAG (sin contacto). b- Vaporización de hueso necrótico maxilar usando láser ER:YAG. c- 1 mes después de la aplicación del láser que muestra una completa curación del sitio tratado en (a). d- 1 mes después de la aplicación del láser, se muestra una completa curación del área maxilar tratada en (b). (Fuente: Biphosphonates and Osteonecrosis of the jaw: A Multidisciplinary Approach. Pag.132) |
Muchos autores han informado como un efecto de la TLBI la angiogénesis y el crecimiento capilar, así como un aumento del factor de crecimiento (TGF, PDGF, Bfgf, IL6, IL8, IL1A). Rápida formación de colágeno tipo I y III y un aumento en la deposición de colágeno también se ha reportado en muchos experimentos en vivo y en vitro. Un efecto significativo de la irradiación con láser, es la actividad antibacteriana mostrada en estudios en vivo, en vitro y en modelos animales. Esto es de relevancia en la ONM, por el hecho de las colonias bacterianas presentes en el biofilm dental como en las zonas óseas expuestas. Así como, la mucosa alrededor de las lesiones necróticas, en donde se encontraron especies de Actinomyces spp, Eikinella, Pepstreptococcus y Legionella. Sin embargo, no está claro si la infección es un evento primario o secundario en la fisiopatología de la ONM
3.
La eficacia del tratamiento láser va a depender de la longitud de onda utilizada, y por lo tanto, en la energía suministrada y las especies bacterianas que están siendo irradiadas. Es importante destacar, que el mecanismo exacto por el cual la radiación láser ejerce su efecto bactericida aún no ha sido determinado, pero probablemente implica efectos fotoquímicos o fototérmicos
3.
En base a la experiencia un estudio llamado "Nd:YAG laser biostimulation in the treatment of bisphosphonate-associated necrosis of the jaw: clinical experience in 28 cases" publicado por Vescovi en (2008) constó en aplicar el láser Nd:YAG para bioestimular la zona afectada por ONM sumado a terapia antibiótica (Amoxicilina 2 gr y 1, 5 gr de metronidazol diario durante 2 semanas). El láser Nd:YAG (longitud de onda de 1.06 nm, potencia de 1,25 W, frecuencia 15 Hz, fibra de diámetro 320- lm) se usó para aplicar TLBI de forma desenfocada a una distancia de 1-2 mm desde el tejido durante 1 min (PD 1865 W/cm2, por fluencia de pulso 124.33 j/cm2, fluencia acumulativa 746 j/cm2) durante cinco aplicaciones consecutivas. De 14 pacientes tratados con TLBI, 9 reportaron una completa recuperación clínica (no había dolor, sin signos de infección o zonas óseas expuestas), y 3 mejoraron sus síntomas con un seguimiento de entre 4 a 7 meses. Esto en contraste de los pacientes restantes que fueron tratados solo con medicamentos, de los cuales ninguno tuvo mejoría significativa
13.
Así mismo, otro estudio publicado por Vescovi en (2011) denominado "Surgical Approach and Laser Applications in BRONJ Osteoporotic and Cancer Patients" se llevo a cabo en pacientes con cáncer y sin cáncer que presentaban ONM. Los pacientes se dividieron en grupos y fueron tratados tanto de la forma convencional como con TLBI. Los resultados indicaron que la cirugía temprana conservadora, usando el láser ER:YAG combinado con TLBI y la antibiótico terapia; indujo la remisión de la ONM en el 90% de los casos de los pacientes con o sin cáncer de forma eficiente. Esto en comparación con el 53 % obtenido con cirugía tradicional (instrumentos rotatorios), mejorando así la calidad de vida de los pacientes de los cuales: en el estadio I hubo un 75% de mejoría, en el estadio II un 54,24% y un 33,3% en el estadio III. En dicho estudio, el láser ER:YAG fué usado con diferentes intensidades; para la resección de las zonas necróticas que eran irrigadas a su vez: con solución yodada y un sistema de agua destilada
14.
En relación a lo antes mencionado, fué hecho un estudio por Pourzarandian (2004) a los pacientes tratados con láser denominado "Histological and TEM examination of early stages of bone healing after Er:YAG laser irradiation". Dicho estudio mostro en el examen histopatológico, predominio de un tejido de granulación rico en fibroblastos y osteoblastos 7 días después de usar el láser. A los 14 días los pacientes tratados con láser Er:YAG mostraron, una significativa nueva formación de hueso en comparación con el grupo tratado con láser CO2
10.
Por su parte, Rugani (2013) llevo a cabo un estudio titulado "Use of Photodynamic Therapy in Treatment of Bisphosphonate-related Osteonecrosis of the Jaws: Literature Review and Case Series" en donde concluyo luego de hacer revisiones de varios autores que la TLBI puede ser usada como tratamiento conservador en pacientes con osteonecrosis inducida por bifosfonatos, por el hecho de que ayuda a mitigar los síntomas, sanar la mucosa y desinfectar la zona afectada. Además, sirve de mucha ayuda cuando los procedimientos quirúrgicos no están indicados y, puede ser usada como complemento antes o después de usar los métodos quirúrgicos convencionales; o como opción primaria en casos de las etapas tempranas de la patología donde la TLBI puede ser suficiente para promover la formación de nuevo tejido de granulación que promueva el cierre del área expuesta descartando la cirugía
15.
CONCLUSIONESA pesar de los muchos informes en la literatura, la terapia óptima de la ONM sigue siendo un tema sin resolver y no hay directrices basadas en la evidencia. La discusión actual gira en torno a dos enfoques opuestos: tratamientos no invasivos vs invasivos. Independientemente de la estrategia elegida, los objetivos principales del tratamiento se enfocan en aliviar el dolor, reducir la infección, estabilizar la progresión de la enfermedad y por supuesto obtener el cierre de la exposición ósea. La terapia con antibióticos representa una solución no invasiva, válida para mitigar los síntomas de la ONM, pero los resultados a largo plazo en relación a la sanación de la mucosa son peores comparados con el abordaje quirúrgico. La Terapia Láser de Baja intensidad permite usar el láser sobre el hueso necrótico expuesto para su desbridamiento quirúrgico, incluso cuando el procedimiento se realice bajo anestesia local. El hueso necrótico es gradualmente vaporizado hasta que alcanza el hueso sano. La técnica mínimamente invasiva de ablasión permite que las superficies óseas seccionadas hacerse regulares. Además de que, se puede utilizar para crear microperforaciones en la base para una nueva vascularización. Otras de las ventajas de la terapia láser son: una acción bactericida y bioestimulante, lo que resulta en una mayor recuperación postoperatoria. Tomadas en conjunto estas consideraciones, resulta eficaz el uso de TLBI en el tratamiento de los defectos mucosos y óseos relacionados a la ONM por el uso de bifosfonatos de forma espontanea o luego de extracciones dentales. Sin embargo, una revisión de la literatura mostró resultados menos satisfactorios para las lesiones de la fase III de la ONM, que para las etapas más bajas (estadios I y II). En base a este resultado, los pacientes con una exposición mínima de hueso deben de ser considerados candidatos para las estrategias quirúrgicas conservadoras con Terapia Láser de Baja Intensidad sumado a la antibiótico terapia.
REFERENCIAS BIBLIOGRÁFICAS
- Yépez J, Páez N, Gottberg E. Osteonecrosis de los maxilares inducida por bifosfonatos. Revista odontológica de los andes [en línea]. 2009 [consulta : enero 10 marzo 2014];4(1):43-54. Disponible: http://www.saber.ula.ve/bitstream/123456789/29020/1/articulo6.pdf
- Sosa M, Gómez MJ, Bagán JV, Díaz M, Díez A, Jódar E, Gutiérrez L, del Pino J, Barrero V. Osteonecrosis de los maxilares: Documento de consenso. Rev Osteoporos Metab Miner [enlínea].2009[consulta:10marzo2014];1(1):41-51.Disponible: http://www.ser.es/ArchivosDESCARGABLES/consensos/Osteonecrosis_de_losmaxilares.pdf
- Lannetti G. : Biphosphonates and Osteonecrosis of the jaw: A Multidisciplinary Approach. Milan- Italy, Springer- Verlag Editorial, 2012.
- Jaimes M, Miranda Ch, Olate S, Miranda M, Albergaria J. Bifosfonatos y osteonecrosis de los maxilares. Consideraciones sobre su tratamiento. Scielo [en línea]. 2008 [consulta: 21 enero2014];26(3):681-688.Disponible: http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0717-95022008000300028
- Atanes P, Atanes A, Rios P, Atanes A. Osteonecrosis de los maxilares relacionada con el tratamiento con bifosfonatos.Semerg [en línea]. 2013[consulta: 21 enero 2014];591(6). Disponible: http://www.elsevier.es/eop/S1138-3593%2813%2900130-5.pdf
- Capote C, Mogensen A, Sanchez Maria, Cedeño J.A. Consideraciones en el tratamiento odontológico de pacientes en terapia con bifosfonatos. Acta odontol venez [en línea].2010[consulta:20mayo2014];49(4). Disponible:http://www.actaodontologica.com/ediciones/2011/4/art21.asp
- Molina W, Sibaja L. Osteonecrosis de los maxilares asociado al uso de bifosfonatos. Revista Medica de Costa Rica y Centro America [en línea]. 2012[consulta: 21 enero 2014];69(600)47-52. Disponible: http://www.binasss.sa.cr/revistas/rmcc/600/art10.pdf.
- Giribone J, Catagnetto P. Osteonecrosis de los maxilares inducida por bifosfonatos; lo que el odontologo debe saber hoy : pautas y protocolos. Scielo [en línea].2013[consulta:1febrero2014];15(21).Disponible: http://www.scielo.edu.uy/scielo.php?pid=S1688-93392013000100006&script=sci_arttext
- Navarro C.: Tratado de cirugía oral y maxilofacial tomo I. Madrid- España, editorial Aran, 2004.
- Pourzarandian A, Watanabe H, Aoki A, Ichinose S, Sasaki K, Nitta H, Ishikawa I . Histological and TEM examination of early stages of bone healing after Er: YAG laser irradiation. Pubmed[en línea].2004 [consulta: 1 febrero 2014].Disponible: http://www.ncbi.nlm.nih.gov/pubmed/15345179
- Leco I, Martínez J, Donado M, López C. Efectos esterilizantes del láser Erbium : Yag sobre las estructuras dentarias: estudio in vitro.Scielo[enlínea].2005[consulta:20enero 2014];11(2). Disponible:http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1698-69462006000200013
- Zevateta D. Aplicaciones del láser Nd: YAG en Odontologia. Scielo[en línea].2004[consulta: 15febrero2014];9(5).Disponible:http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1138-123X2004000500005
- Vescovi P, Merigo E,Manfredi M, Meleti M, Fornaini M, Bonanini M, Rocca JP, Nammour S. Nd: YAG laser biostimulation in the treatment of biphosphonate-associated necrosis of the jaw: clinical experience in 28 cases.Pubmed[en línea].2008[consulta: 21 marzo 2014]. Disponible: http://www.ncbi.nlm.nih.gov/pubmed/18248160
- Vescovi P, Merigo E, Meleti M, Maddalena M, Carlo F, Nammour S. Surgical Approach and Laser Applications in BRONJ Osteoporotic and Cancer Patients. Journal of osteoporosis[enlínea].2011
[consulta:16abril2014];2012(8).Disponible:http://www.hindawi.com/journals/jos/2012/585434/
- Rugani P, Truschnegg A, Acham S, Kimbauer B, Jakse N. Use of Photodynamic Therapy in treatment of Biphosphonate-related Osteonecrosis of the jaws: Literature Review and Case Series. Anal Bioanal Tech[en línea] .2013[consulta: 16 abril 2014];1(6).Disponible: http://omicsonline.org/use-of-photodynamic-therapy-in-treatment-of-osteonecrosis-2155-9872.S1-006.pdf
|

