Recibido para arbitraje: 02/09/2017
Aprobado para su publicación: 01/11/2017
Las deformidades auriculares, son el resultado de alteraciones congénitas, traumas y cirugías de resección oncológica. La perdida de estas estructuras, pueden comprometer la estética y llegan a afectar psicologicamente al paciente, influyendo negativamente en su calidad de vida. El objetivo de este trabajo es mostrar un caso de rehabilitación auricular con prótesis implanto soportada. Paciente de 35 años de edad, portador de deformidad auricular causada por accidente automovilístico, fue sometido a la rehabilitación de la oreja derecha que había sido amputada. La rehabilitación auricular consistió en la instalación de 2 implantes craneofaciales. Después de 6 meses, fue confeccionada la prótesis auricular y durante los 3 años de control clínico, la prótesis conserva sus características anatómicas. Resaltamos que la rehabilitación de defectos auriculares, con prótesis implanto soportadas, muestran resultados estéticos previsibles.
Palabras clave: Deformidades adquiridas del oído, Prótesis implanto soportada, Prótesis auricular
The auricular deformities are the result of congenital alterations, traumas and oncological resection surgeries. The loss of these structures can compromise the aesthetic and come to affect the patient psychologically, negatively influencing their quality of life. The objective of this work is to show a case of auricular rehabilitation with implanto supported prosthesis. A 35-year-old patient, with an auricular deformity caused by a car accident, underwent rehabilitation of the right ear that had been amputated. Auricular rehabilitation consisted in the installation of 2 craniofacial implants. After 6 months, the auricular prosthesis was made and during the 3 years of clinical control, the prosthesis retains its anatomical characteristics. We emphasize that the rehabilitation of auricular defects, with implanted prostheses supported, show predictable aesthetic results.
Key words: Acquired ear deformities, Implant supported prosthesis , Auricular prosthesis
Correspondencia: [email protected]
Las deformidades auriculares, son el resultado de alteraciones congénitas, traumas y cirugías de resección oncológica1. La perdida de estas estructuras, pueden comprometer la estética y llegan a afectar psicologicamente al paciente, influyendo negativamente en su calidad de vida. Frente a esto, pueden ser realizadas cirugías plásticas mediante el uso de injertos, pero en la mayoría de las veces son un tratamiento muy limitado, porque no devuelven las características estéticas que se ha perdido2.
En este contexto, a partir de los conceptos de Oseointegración por el profesor Branemark3, la instalación de implantes craneofaciales puede ser la mejor alternativa para la retención de prótesis auriculares, cuando son comparadas con prótesis que tienen su retención por medio de adhesivos4, que en algunos casos son retenidas juntamente con los anteojos. Por tal motivo, este tipo de prótesiss auriculares implanto soportadas generan mayor confort y calidad de vida para los pacientes. Hoy en día la literatura muestra buenos resultados en la tasa de supervivencia de los implantes craneofaciales instalados en pacientes con deformidad auricular. El presente trabajo ilustra un caso clínico de un paciente portador de deformidad auricular, que fue rehabilitado por medio de una prótesis implanto soportada, enfatizando los aspectos técnicos quirúrgicos, así como la calidad de la prótesis.
Paciente de sexo masculino, 35 años de edad, portador de deformidad auricular causada por accidente automovilístico, fue sometido a la rehabilitación de la oreja derecha que había sido amputada (Figura 1). Considerando la indicación de una prótesis implanto soportada, para planificar la instalación de los implantes, la región del hueso temporal fue examinada mediante una tomografía computarizada, para evaluar el volumen óseo en profundidad.
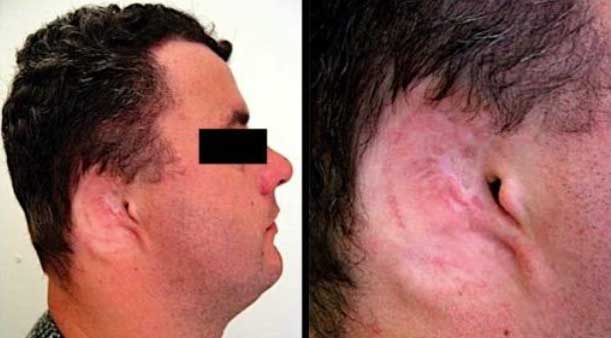
El paciente fue sometido a la cirugía de instalación de los implantes en un quirófano, bajo anestesia general. La rehabilitación auricular consistió en la instalación de 2 implantes craneofaciales (medidas entre 3 a 5 mm X 3.75 mm, Nobel Biocare, Zurich, Swizerland), en la región mastoide del hueso temporal. Se realizó inicialmente una incisión semilunar posterior al conducto auditivo externo de aproximadamente 40 mm. Luego se separó el colgajo cutáneo en toda su dimensión, para iniciar el fresado por medio de una secuencia de fresas escalonadas, que determinaron la profundidad (longitud de los implantes) y su posición final (Figura 2A). Después de las perforaciones, los implantes craneofaciales se instalaron con una baja rotación (10 a 20 rpm) e intensa irrigación con suero fisiológico, quedando los implantes a unos 20 mm posterior del conducto auditivo externo (Figura 2B). Los remanentes auriculares fueron extirpados y el grosor de tejido cutáneo alrededor de los implantes fue diminuído, con la idea de proporcionar una piel mas firme e inmóvil alrededor de los pilares de cicatrización, minimizando las reacciones cutáneas. Los pilares de cicatrización (Nobel Biocare) se atornillaron sobre los implantes y fueron apretados con un torque de 15 Ncm. Durante 2 semanas se mantuvo un apósito compresivo, por medio de gasa embebida en una pomada de corticoide + antibiótico (hidrocortisona + oxitetraciclina – terra-cortril), con el fin de mantener la piel comprimida contra el periostio. El tiempo de cicatrización de los implantes fue de 3 a 6 meses, durante ese período el paciente fue examinado la 1ra. y 2da. semana después de la cirugía, y posteriormente cada 3 meses para verificar el proceso cicatricial.
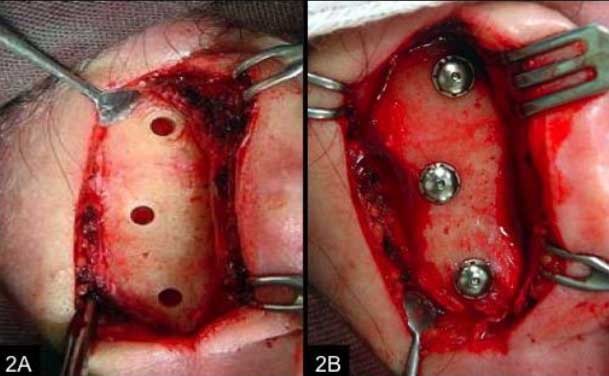
Después de 6 meses, la prótesis auricular fue diseñada por el protesista. Inicialmente, se realizó una impresión de la región auricular, seguidamente se obtuvo un modelo de yeso con los análogos de los implantes. Un puente metálico fue confeccionado y atornillado sobre los implantes. La prótesis fue tallada en cera y probada en el paciente, donde se verifico la forma, el tamaño, la posición y la estética. La prótesis definitiva fue fabricada en material de silicona (VST50F, Factor II, Lakeside, AZ) y coloreada intrínsecamente. Después de la completa polimerización de la silicona, la prótesis fue retirada del molde de yeso, recortada, coloreada extrínsecamente y probada en el paciente, para la verificación estética (Figura 3). El paciente recibió instrucciones de higiene local en el momento de la entrega de las prótesis. Estas orientaciones consistieron en la limpieza diaria de los puentes, mediante la remoción mecánica y química utilizando cepillos infantiles, también fue orientado a no dormir con la prótesis. Se examino al paciente semanalmente por un mes, después cada mes por 6 meses y al final cada año. Durante los demás años, el paciente fue examinado anualmente por el protesista y cirujano, después de 3 años de control clinico, la prótesis presentó buen estado de conservación.
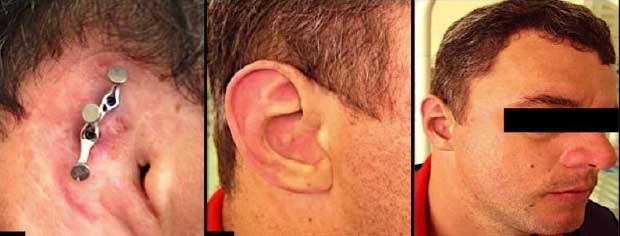
El presente caso clínico muestra una rehabilitación con implantes extraorales, siendo una alternativa valiosa, para los pacientes portadores de defectos auriculares. Cuando se evalúa el concepto de osseointegración propuesto por Brånemark y Albrekttsson para la rehabilitación craneofacial, observamos resultados previsibles para la retención de las prótesis craneofaciales3,5,6,7.
Cuando consideramos las demás modalidades terapéuticas, como las cirugías reconstructivas utilizando el tejido autógeno, la principal limitación es la obtención de un resultado estético satisfactorio, pues es imposible reproducir anatómicamente la oreja utilizando un tejido autógeno2. Además, el éxito es imprevisible considerando calidad del injerto, condiciones de vascularización y factores cicatriciales. En comparación a las otras modalidades de rehabilitación, a través de las prótesis auriculares implanto soportadas, es posible obtener mejor retención, fácil colocación, mayor satisfacción, confort y mejora de la calidad de vida de los pacientes8,9,10,11,12.
Considerando la calidad de vida de pacientes portadores de deformidades faciales, las prótesis implanto soportadas, han ganado una importante aceptación para este tipo de rehabilitación, principalmente por el resultado estético que la calidad del material proporciona. Además, desde el punto de vista clínico, la buena retención de la prótesis es crucial para la comodidad del paciente10,11,12.
La literatura señala que la tasa de supervivencia de los implantes extraorales a largo plazo, son tan favorables como los resultados de los implantes instalados en la cavidad oral13,14,15,16,17. Sin embargo, algunos estudios mostraron diferencias de éxito, cuando los implantes fueron instalados en distintas regiones anatómicas6,18. Comparando con otras regiones faciales, la región auricular presenta mejores resultados cuando son comparados con la region orbitaria6,18. Los critérios para la tasa de exito de los implantes craneofaciales son: la cantidad y calidad ósea de la región, grosor de la piel alrededor de los implantes, calidad de higiene local y tratamiento de radioterapia previa6,19.
Los pacientes oncológicos con deformidades auriculares, que son sometidos a radioterapia, pueden presentar mayores posibilidades de fracaso durante la oseointegración, como consecuencia de los efectos progresivos de la radiación ionizante18,20. Aunque, tambien existe evidencia mostrando resultados favorables, para los implantes instalados en tejido irradiado20. Ya en los casos de deformidades congénitas o trauma, la tasa de éxito es mayor debido a que el hueso es mas saludable6,19.
Aunque los estudios demuestren éxito en la rehabilitación a través de prótesis implanto soportadas, es importante considerar los aspectos negativos que contribuyen a la perdida de los implantes como son: la calidad y cantidad de tejido óseo, la falta de higiene local y radiación. La falta de oseointegración del implante está fuertemente relacionada con la cantidad insuficiente de hueso compacto, que proporciona estabilidad primaria en el momento de la inserción del implante. La higiene local, es un factor primordial en el mantenimiento del tejido sano alrededor de los implantes5,6,11. La inflamación crónica de los tejidos blandos peri-implantarios puede causar la falla del implante21. En el seguimiento de este caso clínico, se han reforzado las instrucciones de higiene, con el fin de promover buenos resultados a largo plazo22,23.
A partir de este trabajo, se puede concluir que la rehabilitación de defectos auriculares a través de prótesis implanto soportada es un método seguro, confiable y previsible para restaurar la apariencia normal del paciente, ofreciendo una mejora en la calidad de vida.