Recibido para Arbitraje: 29/05/2018
Aceptado para Publicación: 05/06/2018
La hipersensibilidad dentinaria (HD) se define como dolor agudo breve ocasionado por la exposición de la dentina en respuesta a estímulos típicamente térmicos, evaporativos, táctiles, osmóticos o químicos que no puede ser atribuido a ninguna otra patología o defecto dental. La teoría hidrodinámica es la más aceptada para explicar esta condición. Las posibles causas de la aparición de la HD son la abrasión, abfracción, atricción, la erosión dental, la recesión gingival, la enfermedad periodontal y su tratamiento quirúrgico o no quirúrgico. A pesar de los efectos benéficos que tienen los tratamientos para contrarrestar la enfermedad periodontal, el raspado, alisado radicular y la cirugía periodontal, pueden conducir a los síntomas de HD, aunado a las técnicas incorrectas de higiene bucal o hábitos alimenticios inadecuados por parte de los pacientes. En esta investigación se realizó una revisión documental con el objetivo de describir las características de la HD y su enfoque desde el punto de vista periodontal.
Palabras clave: hipersensibilidad dentinaria, sensibilidad radicular, hipersensibilidad cervical, raspado y alisado radicular, cirugía periodontal.
Dentin hypersensitivity (DH) it is defined as a brief sharp pain which is caused by the dentin’s exposition as a response to typically thermal stimulus, evaporative, tactile, osmotic, or chemicals, which cannot be attributed to any other pathology or dental flaw. The hydrodynamic theory is the most accepted in order to explain this condition. The possible causes of DH manifestation are the abrasion, abfraction, attrition, dental erosion, the gingival recession, the periodontal disease and its surgical or not surgical treatment. Despite the beneficial effects the treatments have to counter the periodontal disease, scaling, root planning and periodontal surgery, can lead to DH symptoms, along with wrongful techniques of mouth hygiene or inadequate eating habits on behalf of the patients. On this research, a documentary review was made with the objective of describing DH’s characteristics and its approach from a periodontal point of view.
Key words: Dentin hypersensitivity, root sensitivity, cervical hypersensitivity, scaling, root planning, periodontal surgery
Correspondencia: Cátedra de Periodoncia UCV. Ciudad Universitaria. Caracas 1060.
La hipersensibilidad dentinaria (HD) es un dolor localizado, sostenido, de corta duración, causado por cambios térmicos, táctiles y estímulos osmóticos. Generalmente la definición está aplicada a la exposición cervical de la dentina1. Esta entidad puede afectar al 20,6% de la población, presentando una alta predilección por edades comprendidas entre los 36 a 45 años, siendo el género femenino el más comprometido2. La teoría hidrodinámica postula que la mayoría de los estímulos que producen dolor aumentan el flujo centrífugo de los fluidos en los túbulos, causando un cambio de presión en toda la dentina, lo que activa los nervios interdentales en el límite pulpo-dentinario o dentro de los túbulos dentinarios. Se ha establecido que esta estimulación ocurre a través de una respuesta mecano-receptora que distorsiona los nervios pulpares3.
Abrasión: Es definida como el desgaste patológico de la superficie dental debido a un proceso mecánico de fricción, como por ejemplo el cepillado dental: La frecuencia, tipo de cepillo dental y grosor de los filamentos. El tipo de pasta dental también está directamente relacionado con esta lesión4, sin embargo la HD parece relacionarse más con la frecuencia de cepillado y la ejecución de una técnica horizontal que con el tipo de crema dental o la dureza de las cerdas5.
Erosión dental: Se asocia a procesos electrolíticos o químicos donde el cepillado actúa como coadyuvante. La erosión se produce por causas químicas sin participación microbiana6. Estos ácidos pueden ser de origen interno (jugo gástrico)7 o externos (dieta)8. El ácido de las bebidas puede remover el barrido dentinario creado sobre las superficies dentarias durante el raspado y alisado radicular propiciando la apertura de los túbulos dentinarios9.
Abfracción: son aquellos defectos en cuña que aparecen en la unión amelocementaria, su etiología se fundamenta en la hipótesis que las fuerzas oclusales excéntricas generan flexiones del diente en la zona cervical y microfracturas que determinan la morfología característica de estas lesiones10.
Atricción: Es un proceso mecánico que involucra contacto diente con diente. La atrición fisiológica es la pérdida regular gradual del diente como consecuencia de la masticación fisiológica pudiendo afectar todas sus superficies. Por otra parte, la atricción patológica es causada por una función anormal o por la inadecuada posición de los dientes, limitada a un diente o a un grupo de estos que evidencian alteraciones de la oclusión11. Este proceso está asociado con la función oclusal exagerada por hábitos parafuncionales como el bruxismo12. Una minuciosa historia clínica sobre alteraciones de pH, flujo salival, hábitos dietéticos y técnicas de cepillado pueden diferenciar estas lesiones en sus etapas iniciales11.
Características anatómicas de la unión cemento-esmalte: El cemento que se haya en esta unión o inmediatamente subyacente a esta tiene una importancia clínica particular durante el tratamiento periodontal. En la unión amelocementaria el cemento presenta relaciones de tres tipos. En el 60 a 65% de los casos el cemento se superpone al esmalte, cerca de un 30% la unión tiene lugar borde a borde y en un 5-10% el cemento y el esmalte no están en contacto. En este último caso, la recesión gingival genera HD por exposición de la dentina13,14.
Recesión gingival: Es definida como una condición clínica libre de inflamación, caracterizada por la migración apical de la encía vestibular y menos frecuentemente en la zona palatina o lingual15. Ha sido considerada un enigma en la etiología multifactorial de la HD16. Esta lesión aumenta en prevalencia y gravedad, en función con la edad del individuo17. Puede aparecer como consecuencia de la enfermedad periodontal y su tratamiento11.
Se reportan varios factores anatómicos que pueden predisponer a la aparición de la recesión gingival: raíces prominentes en presencia de una mucosa delgada, dehiscencias o fenestraciones en la tabla ósea, inserción baja de frenillos, movimientos ortodónticos que colocan las raíces fuera de la tabla ósea vestibular18. Los dientes donde se presentan mayores recesiones son los primeros premolares, caninos y segundos premolares superiores seguidos por los incisivos superiores izquierdos, esto coincide con los dientes con mayor reporte de HD19.
Enfermedad Periodontal y su tratamiento: La HD es un problema relativamente frecuente en la práctica periodontal20. Se puede presentar de manera espontánea cuando la raíz se expone como resultado de la recesión gingival o formación de sacos periodontales, o bien puede aparecer después del raspado, alisado radicular y otros procedimientos quirúrgicos21.
El raspado y alisado radicular es un procedimiento indispensable para el tratamiento de la enfermedad periodontal. Sin embargo, no solo los depósitos microbianos serán eliminados de la superficie radicular, sino también el cemento y parte del tejido dentinario22, por lo tanto, mediante esta instrumentación, se expondrán los túbulos dentinarios al medio bucal quedando frecuentemente la dentina sin protección. La colonización microbiana posterior en la dentina radicular expuesta puede originar la invasión hacia los túbulos dentinarios y como consecuencia, pueden generarse lesiones inflamatorias en la pulpa23.
El raspado y alisado de la superficie dental no sólo deja una capa de frotis, sino que las bacterias pueden ser “forzadas” a entrar en los túbulos por la acción de la instrumentación. Se ha demostrado que los dientes con un compromiso periodontal, tienen un mayor porcentaje de bacterias viables dentro de los túbulos dentinarios, lo que puede causar una respuesta inflamatoria dentro de la pulpa que se manifiesta como sensibilidad radicular. Esto sugiere que la presencia de HD en las superficies radiculares expuestas después de la terapia periodontal puede ser una condición distinta a la HD que ocurre después de la teoría hidrodinámica por la penetración bacteriana en los túbulos dentinarios abiertos24.
Los pacientes que asisten a consultas periodontales y reciben terapia periodontal pueden ser cuatro veces más propensos a sufrir HD postoperatoria que aquellos que acuden al odontólogo general, esto hace pensar que el tratamiento de la enfermedad periodontal puede jugar un papel en la etiología de la HD25,26. Para describir la sensibilidad de los dientes con enfermedad periodontal, antes y después de una terapia quirúrgica o no quirúrgica fue acuñado el término sensibilidad radicular27. Este término se adoptó a consecuencia de la sensibilidad producida por la enfermedad periodontal y su tratamiento, asociada a la invasión bacteriana dentro de los túbulos dentinarios hasta una profundidad próxima a la pulpa24, no obstante, el término "hipersensibilidad dentinaria" fue el propuesto y adoptado por el Consenso Internacional Canadiense en el año 2003, independientemente de su origen28.
Después de realizar la terapia periodontal no quirúrgica la dentina se expone y sus túbulos quedan abiertos, por lo que se incrementa la permeabilidad de la misma y el paciente refiere hipersensibilidad29. Diversos estudios clínicos determinan la prevalencia de la HD en la población de pacientes que asisten a la consulta de periodoncia30,31. Esto sugiere que la enfermedad periodontal y su tratamiento pueden jugar un rol importante en la etiología de la HD donde la biopelícula dental como agente etiológico de la HD es un área de interés32.
El estudio realizado en Sao Paulo, Brasil por Sobral et al6, reportaron que de 32 pacientes que manifestaron HD, el 41% había sido sometido a tratamiento periodontal en meses anteriores a la evaluación y a un 29% se les había realizado una cirugía periodontal. Fogel et al33, realizaron un estudio con el propósito de cuantificar los efectos del raspado radicular en la permeabilidad de la dentina en la raíz de terceros molares. Se removieron las coronas y se hicieron cortes longitudinales de la raíz. Se midió la conductancia hidráulica de la dentina antes y después del raspado radicular, luego se sometieron a grabado ácido y a la aplicación de oxalato de potasio utilizando un método de filtración de fluidos. Los resultados mostraron que el raspado radicular crea una capa de frotis que reduce la permeabilidad de la dentina subyacente, sin embargo, este frotis es lábil a los ácidos, por lo tanto, el raspado radicular puede causar una mayor permeabilidad en la dentina con la consecuente HD, invasión bacteriana de los túbulos e irritación de la pulpa33.
De acuerdo al estudio, de Taani et al34, los pacientes remitidos al servicio de Periodoncia tienen una prevalencia de HD significativamente mayor (60,3%) que los examinados en el servicio de odontología general (42,4%). La recesión gingival asociada a los dientes hipersensibles fue significativamente mayor en los pacientes del servicio de Periodoncia que los pacientes evaluados en el servicio de odontología general (p <0,01). La asociación de la enfermedad periodontal y el tratamiento periodontal con una alta prevalencia de HD y recesión gingival en pacientes referidos al periodoncista sugeriría una relación de la enfermedad periodontal y la HD34.
Tammaro et al22, realizaron un ensayo clínico basado en la observación de treinta y cinco (35) pacientes con HD que se presentó una semana después de haber realizado el raspado y alisado radicular. Después de tres semanas de instrucciones para la eliminación de la biopelícula dental, registraron una disminución de la HD. Concluyeron que una cuidadosa higiene puede ayudar en la disminución de la HD mientras que el raspado y alisado radicular puede actuar como desencadenante de esta condición22, no obstante, posterior al tratamiento periodontal se evidencia de manera frecuente una sensibilidad temporal al calor o frío, que tiende a disminuir si se mantiene un estricto control de la biopelícula dental. De no existir tal control, la HD permanecerá o incluso podría aumentar35.
Una gran cantidad de estudios asociados con la terapia periodontal ha mostrado interés en la disminución de la biopelícula dental, control de la inflamación, reducción de la profundidad de los sacos periodontales, cambios que se suceden en la flora microbiana y los parámetros deseables, sin embargo, desde la perspectiva del paciente no han sido estudiados en amplitud33.
Durante la fase de mantenimiento de la terapia periodontal, el raspado y alisado radicular es con frecuencia, un procedimiento repetido. En cada sesión de control se desbridan las raíces y se elimina parte la dentina. Esta terapia puede debilitar no solo la estructura dentaria, sino además puede generar la formación de gran cantidad de dentina reparadora36. Haugen et al37, realizaron el estudio de un caso, donde reportan un incremento de la HD después de la fase de mantenimiento. El procedimiento incluyó la extracción de los molares y su análisis bajo microscopio electrónico, observándose zonas donde los túbulos dentinarios se veían claramente. Concluyen que la instrumentación periodontal repetida puede desencadenar la aparición de la HD37.
Romero et al38, realizaron un estudio piloto para observar la frecuencia de la HD posterior al raspado y alisado radicular en cuarenta y nueve (49) pacientes que asistieron al Postgrado de Periodoncia de la Facultad de Odontología de la UCV de los cuales solo catorce (14) cumplieron con los criterios de inclusión y exclusión, la evaluación fue registrada en una encuesta diseñada para tal fin y aplicada a las tres semanas del procedimiento. De acuerdo a los resultados obtenidos sugieren que en la población estudiada el raspado y alisado radicular pudiera ser un factor desencadenante de la HD38.
Wallace et al39, hicieron un estudio para determinar cambios significativos en la HD después de la tartrectomía, raspado y alisado radicular y cirugía periodontal. Evaluaron ochenta y cuatro (84) dientes premolares y molares, cuarenta y dos (42) controles y cuarenta y dos (42) experimentales a los cuales le realizaron pruebas con estímulos al frío y al aire. Los resultados obtenidos arrojaron que la hipersensibilidad se incrementó en todos los casos después de la cirugía, asociada al grado de exposición radicular. Por otra parte los pacientes tratados con colgajos reposicionados apicalmente y osteotomía presentaron mayor hipersensibilidad al estímulo de aire que los sometidos a colgajo de Widman modificado39.
Canakci et al40, evaluaron los niveles de molestia que experimentaron cincuenta y seis (56) pacientes con periodontitis crónica después de procedimientos quirúrgicos periodontales (colgajo de Widman modificado, colgajo con resección ósea y gingivectomía), a partir de una escala de valoración numérica, registrando la percepción de cada paciente después de ser estimulado con aire. En sus resultados reportaron que todos los pacientes experimentaron dolor después de los procedimientos quirúrgicos periodontales, la cirugía periodontal que produjo más sensibilidad fue el colgajo con resección ósea, siendo mayor la HD en los pacientes sometidos a cirugía que los tratados con raspados radiculares no quirúrgicos y la HD era mayor en los pacientes más ansiosos y más jóvenes, debido posiblemente a que a mayor edad, existe mayor formación de dentina secundaria y disminución de la vascularización de los tejidos40.
Tanto el raspado y alisado radicular, como el acondicionamiento de la superficie dental con ácido y el inadecuado tratamiento del área intervenida propician zonas no protegidas por el colgajo. Esta exposición facilita la agresión microbiana41. En este sentido Hastings25 sugiere que la HD posterior a la realización del raspado y alisado radicular perdura algunos días o semanas, mientras que después de una cirugía periodontal, especialmente para aumento de corona o eliminación quirúrgica de sacos periodontales, se presenta una HD más prolongada que puede durar meses o perpetuarse indefinidamente a menos que sea tratada de forma definitiva.
Al-Sabbagh et al42, evaluaron la incidencia y progresión de la HD durante seis semanas consecutivas, en diez (10) pacientes a quienes les realizaron colgajos periodontales. La HD fue evaluada utilizando la sonda Yeaple®, la estimulación fue a través del aire expelido de la jeringa triple y de acuerdo a una escala analógica visual. Concluyeron que la HD se incrementa entre la primera y tercera semana posterior a la intervención quirúrgica y gradualmente decrece sin necesidad de tratamiento desensibilizante42. Por otra parte Lin y Gillam43, en una revisión sistemática encontraron una prevalencia de HD posterior a la terapia periodontal no quirúrgica entre 62.5% y 90%, al día siguiente de realizar el tratamiento, decreciendo entre 52.6% y 55% una semana después. La HD posterior a la cirugía periodontal se presentó entre un 76.8% y 80.4% al siguiente día del procedimiento y fue decreciendo a 36.8% a la semana, 33.4% a las 2 semanas, 29.6% a las 4 semanas y 21,7% a las 8 semanas, considerando que la HD posterior a la terapia periodontal puede ser moderada y transitoria43.
Romero et al44, evaluaron la información que poseen los periodoncistas con respecto a la HD, posterior a la realización de procedimientos quirúrgicos, encontrando que el 89,53% de los encuestados manifestó que sus pacientes refieren HD posterior a la terapia periodontal quirúrgica, siendo la cirugía para reducción de sacos la que genera mayor HD44.
El tratamiento de la HD está basado en el correcto diagnóstico por parte del profesional quien debe estar atento a la existencia de otras condiciones clínicas con características similares45. La estrategia del tratamiento debe comenzar desde la prevención, el autocuidado por parte del paciente en su hogar, complementándola con una intervención particular del profesional dependiendo de la severidad del caso46. Se debe proporcionar un plan de tratamiento que comience con opciones menos invasivas y se intensifique solo cuando esas alternativas hayan demostrado ser insuficientes para aliviar los síntomas del paciente. Por ende, solo después que los métodos no invasivos no hayan logrado reducir los síntomas, pueden considerarse opciones de tratamiento más invasivas, como la cobertura radicular47. En la literatura han sido publicados varios algoritmos clínicos como un sistema simplificado para el abordaje terapéutico de la HD (Figura 1)48.
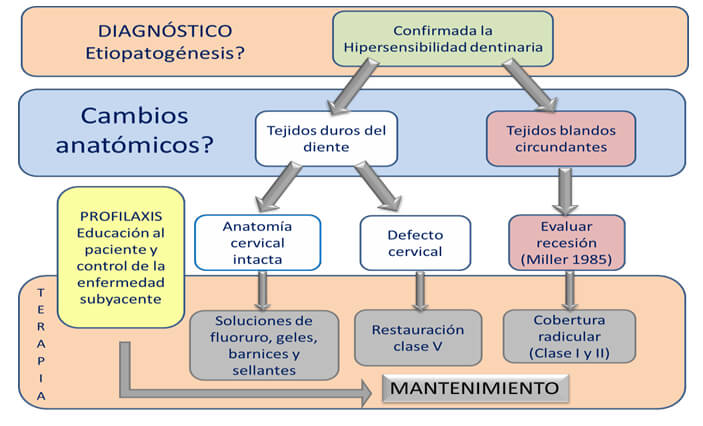
Todo enfoque terapéutico de la hipersensibilidad dentinaria debe estar precedido de un análisis cuidadoso de las condiciones causales o contribuyentes de los distintos síntomas11. Además, es aconsejable el asesoramiento dietético a los pacientes, para evitar el consumo excesivo de cítricos, alimentos y bebidas de naturaleza ácida, el cambio del cepillo de filamentos duros por uno de filamentos suaves y evitar pastas dentales con componentes abrasivos49, para así cumplir con la fase preventiva e identificar el agente etiológico y eliminarlo11. Attin50 aconseja realizar el cepillado una hora después de la ingesta de ácidos.
Un factor importante para reducir o eliminar la HD es el control adecuado de la biopelícula dental, sin embargo, la HD puede impedir la remoción de la biopelícula y por lo tanto se crea un círculo vicioso donde al aumentar la HD, se acumula mayor cantidad de biopelícula y viceversa22. La combinación de erosión ácida y abrasión por cepillado es de importancia en la apertura de los túbulos dentinarios, esto determina la aparición de la HD, por lo cual se deben emplear métodos de higiene lo menos abrasivos posibles con el fin de preservar la integridad de los tejidos dentales cervicales51.
El aumento en el número de pacientes con recesión gingival, sus efectos estéticos desfavorables y su condición como favorecedora de retención de biopelícula dental, cálculo e HD, hacen necesario un cambio en las prioridades terapéuticas inclinadas a la prevención para evitar las causas que puedan provocar la recesión gingival. Si a lo anterior se le añade la dificultad del tratamiento de esta entidad, así como lo reservado de su pronóstico, se observa que la prevención es el único camino que se dirige a solucionar esta problemática52,53.
Una relación de trabajo conjunta entre el profesional de la odontología y el paciente, para cambiar el comportamiento de éste último, es esencial para que la HD sea tratada con éxito54. Drisko55 propone varias sugerencias tanto para el paciente como para el profesional para prevenir la aparición de la HD (Tabla I).
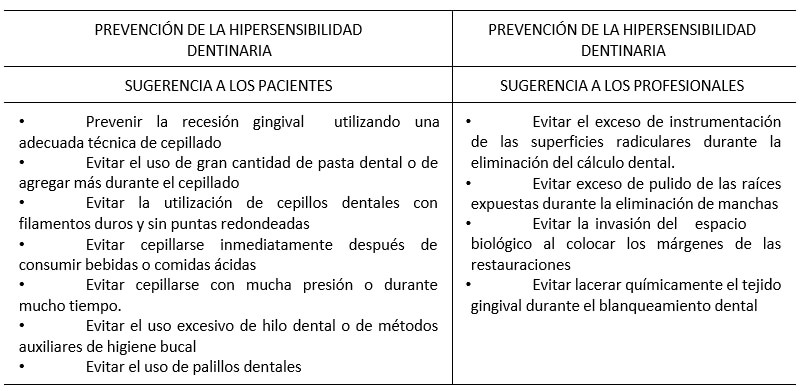
Se ha establecido, que la instrumentación moderada completa con ultrasonido es tan eficaz como la instrumentación manual para eliminar la biopelícula dental, el cálculo y las endotoxinas de las superficies radiculares. La sensibilidad post-operatoria puede ser reducida a través de una cuidadosa instrumentación subgingival y evitando el raspado supragingival exagerado desde el margen gingival hacia la corona55, por lo que Hastings25, recomienda evitar una instrumentación excesiva de las superficies radiculares, especialmente de aquellas con exposición clínica.
Como alternativa al exceso de instrumentación, se dio a conocer un dispositivo que por la acción de un movimiento de burbujeo ultrasónico, provoca la eliminación del cálculo dental, sin tocar a la raíz, por lo tanto sin dolor y sin HD postoperatoria. El sistema Durr Vector® es un aparato que consta de un instrumento muy delgado, como una sonda periodontal, el cual se introduce en el interior de los tejidos, con un movimiento vertical que no toca en absoluto al tejido de la raíz dentaria. Posee gran irrigación, en la cual el agua a presión sumada al efecto de cavitación transmitida al líquido, es similar al burbujeo de un hidromasaje, por lo que desprende el cálculo, pudiéndole colocar diferentes líquidos como antimicrobianos y antisépticos para que actúen en el interior de los sacos periodontales y eliminar así microorganismos residuales. El efecto además consiste en la expulsión de hidroxiapatita a presión y su penetración en la raíz dentaria, irriga y desinfecta la zona, fortalece el cemento y persigue la regeneración ósea alveolar, elimina los microorganismos, cálculo y toxinas sin tocar al diente. No requiere anestesia56.
Dentro de la terapéutica de tratamiento de la HD están los agentes desensibilizantes, los cuales se han clasificado de diversas maneras. De acuerdo a su mecanismo de acción: a) oclusores de los túbulos dentinarios, lo cual previene el movimiento del fluido en su interior y b) despolarizadores de la fibra nerviosa a través de la difusión directa de iones (incrementando la concentración de iones de potasio). Dependiendo de sus propiedades: a) agentes químicos: cloruro de estroncio, nitrato de potasio, citrato de sodio, oxalato férrico y fluoruros, los cuales pueden ejercer uno o ambos mecanismos de acción descritos y b) agentes físicos: destinados a bloquear los túbulos dentinarios como resinas, barnices, sellantes o ionómero de vidrio, sin embargo, muchos de esto agentes proporcionan resultados temporales. Los agentes desensibilizantes también se han clasificado sobre la base de su producto químico y propiedades físicas11. Tabla II
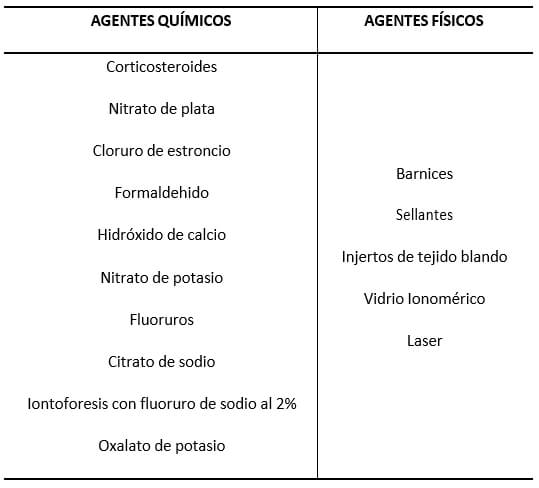
Kopycka-Kedzierawski et al57, evaluaron a través de un cuestionario el manejo que los profesionales de la odontología le dan a la HD. El tratamiento más utilizado fue el nitrato de potasio seguido de los fluoruros. En general, la terapia conservadora para la HD de uso tópico con agentes desensibilizantes pude ser aplicada por el profesional o indicada al paciente para uso en el hogar. Es importante resaltar que el agente desensibilizante ideal no debe ser irritante, no debe poner en peligro la integridad de la pulpa, su aplicación debe ser relativamente indolora, debe aplicarse fácilmente, su acción debe ser permanentemente efectiva y no debe afectar la estructura dentaria57.
Espinoza et al58, utilizaron dentífricos que contenían arginina al 8% con carbonato de calcio versus acetato de estroncio posterior a la terapia periodontal no quirúrgica, encontrando que la HD se redujo tras la primera y la tercera semana en ambos grupos sin diferencias significativas en el efecto de los dos productos. Romero et al44, identificaron cuáles eran los tratamientos más utilizados por 86 periodoncistas de la Sociedad Venezolana de Periodontología en el manejo de la HD, encontrando que un 96.10% de los especialistas entrevistados confirmó la utilización de algún tratamiento para la hipersensibilidad dentinaria. En relación a el tratamiento más utilizado, el 53,24% aplicaron pastas desensibilizantes posterior a la fase periodontal quirúrgica.44
Giassin et al59, proponen prevenir la aparición de HD antes de la terapia quirúrgica y no quirúrgica periodontal utilizando la combinación de productos desensibilizantes (arginina al 8% y carbonato de calcio) tanto en el consultorio como en el hogar. En su estudio, utilizaron estos productos antes de los procedimientos operatorios y luego los pacientes se cepillaban 2 veces al día con el producto. La disminución de la HD se mantuvo durante las diecisiete (17) semanas siguientes a la intervención quirúrgica y no quirúrgica, comparados con un grupo control que utilizó pasta dental con flúor únicamente59.
El láser se ha empleado como un agente físico para el bloqueo de los túbulos dentinarios, el cual parece proporcionar resultados satisfactorios60. Igualmente, se han sugerido los procedimientos quirúrgicos periodontales, para el tratamiento de la HD, tales como: injertos de tejidos conectivos61 y regeneración tisular guiada utilizando membranas reabsorbibles en el caso de recesiones localizadas18. Cuando se considera la realización de una cirugía mucogingival para eliminar la HD se debe tomar en cuenta la clasificación de recesiones gingivales propuesta por Miller62, el número de dientes involucrados en la recesión, la calidad de la encía y el sitio donador18.
Drisko55 sugiere que las recesiones de 1 mm o menos que presenten HD pueden ser tratadas con la corrección de las técnicas de higiene bucal en conjunto con desensibilizantes. Acota que se debe hacer una evaluación periodontal para determinar la factibilidad de la cobertura radicular a través de la cirugía antes de realizar algún procedimiento restaurador que busque reducir la HD debido a que estos materiales pueden influir negativamente en el futuro injerto que se necesite colocar55.
Douglas et al63, realizaron una revisión sistemática para determinar si la cobertura radicular de forma quirúrgica puede reducir la HD, concluyendo que este procedimiento no es predecible debido a que la cobertura radicular se podría dar de forma incompleta. Douglas et al64, evaluaron a través de un cuestionario la calidad de vida de veinticinco (25) pacientes con HD y recesiones gingivales clase I y II a quienes se les realizaron cirugía periodontal (colgajo reposicionado coronalmente con injerto de tejido conjuntivo subepitelial), registrando parámetros periodontales y el grado de HD después de tres meses de haber sido intervenidos, concluyendo que cubrir la recesión gingival quirúrgicamente puede influir positivamente en la calidad de vida del paciente.
Agossa et al65, analizaron, a través de una revisión sistemática, la efectividad de la combinación del tratamiento restaurador con el quirúrgico para tratar lesiones cervicales no cariosas. Concluyeron que los datos para apoyar o refutar este tipo de tratamiento aún están limitados.
Ramireddy et al66, realizaron un estudio clínico en el que compararon el tratamiento de recesiones clase I y II de Miller con colgajos reposicionados coronales acompañados de fibrina rica en plaquetas y colgajos reposicionados coronales en combinación con materiales restauradores en lesiones cervicales no cariosas con presencia de HD. Los resultados demostraron que ambos grupos obtuvieron buena ganancia de tejido queratinizado y ganancia de inserción clínica, sin embargo el grupo que fue tratado con el colgajo reposicionado coronal combinado con material restaurador presentó mayor disminución en la HD66.
Aroca67 afirma que la alta predictibilidad de los tratamientos quirúrgicos (técnica del colgajo reposicionado coronal o técnica del túnel modificado avanzado coronalmente) para cubrimiento radicular hace que este “tratamiento invasivo” sea una buena alternativa para tratar HD considerando que la gran mayoría de estos pacientes presentan recesión gingival. La estabilidad a largo plazo de estas técnicas, en combinación con los cuidados propios del paciente y un correcto mantenimiento permitirán el control de la HD en el tiempo, ofreciendo así una excelente relación entre la morbilidad y el beneficio obtenido67. Serrano et al68, proponen el manejo de la HD según sea localizada o generalizada (Figura 2 y 3)
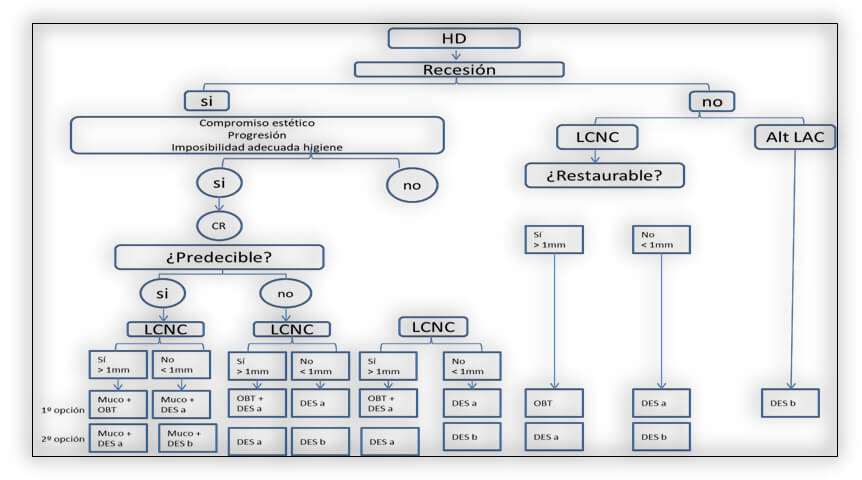

A diferencia de otras áreas de la periodoncia, no existe un modelo de estudio que permita evaluar correctamente la eficacia de los tratamientos orientados a eliminar la HD, ni se dispone de escalas o métodos de estimulación apropiados y reproducibles69, por lo que se deben orientar los esfuerzos a homogeneizar los estímulos empleados para evaluar la hipersensibilidad dentinaria, los métodos de cuantificación, el diseño de estudios clínicos y las opciones terapéuticas menos invasivas. En este sentido se propone la creación de un grupo de estudio con diferentes especialidades que puedan calibrarse y aportar desde sus diferentes puntos de vista como realizar una adecuada evaluación diagnóstica y terapéutica.
La implementación de las nuevas modalidades de tratamiento debe incluir la percepción del paciente sobre el resultado del tratamiento70, por lo que se sugiere la incorporación de la evaluación de la calidad de vida del paciente y su relación con la HD. Es relevante tomar en cuenta las expectativas que tenga el paciente, debido a que la medición de la HD es subjetiva, por ende es bueno conocer qué espera el paciente como resultado de su tratamiento.
Se han publicado numerosos estudios que han demostrado la efectividad de diferentes agentes para el tratamiento de la HD54, sin embargo, ningún tratamiento permite eliminar este problema en todos los pacientes. Además, los resultados de los diferentes estudios y el dolor referido en diferentes personas son muy difíciles de comparar17, los métodos utilizados para la medición del dolor causado por la HD siguen siendo muy subjetivos, por lo tanto los resultados no tienen una base científica sólida. Con relación a este punto es mejor enfocarse en la prevención de la aparición de la HD debido a que no se tiene la certeza que después de instaurada pueda ser eliminada en su totalidad.